Eine Studie mit Talquetamab und Teclistamab jeweils in Kombination mit einem PD-1-Inhibitor (Programmed Cell Death Receptor-1) zur Behandlung von Teilnehmern mit rezidiviertem oder refraktärem Multiplem Myelom (TRIMM-3)
Organisatorische Daten:
| Prüfplancode: | CR109168, 64407564MMY1005 |
| ISRCTN: | |
| EudraCT: | 2021-005073-22 |
| Clinicaltrials.gov: | NCT05338775 |
| DRKS: | |
| Sponsor: | Janssen |
| Studienphase: | 1 |
| Status: | Rekrutierung läuft, geplant bis Sept. 2024 |
Ziel:
Ziel der Studie ist es, die sichere Dosis bzw. sicheren Dosen eines PD-1-Inhibitors in Kombination mit Talquetamab oder Teclistamab zu ermitteln und die Sicherheit und Verträglichkeit von Talquetamab oder Teclistamab bei Verabreichung in Kombination mit einem PD-1-Inhibitor zu charakterisieren.
Hintergrund:
Talquetamab ist ein humanisierter monoklonaler Antikörper, der gegen zwei Ziele gerichtet (bispezifisch) ist: gegen humanes CD3, ein Oberflächenantigen auf T-Zellen, und gegen GPRC5D, ein Antigen in Tumorzellen oder auf deren Oberfläche (tumor-assoziiertes Antigen). Bei Verabreichung bindet Talquetamab sowohl an CD3 auf T-Zellen als auch an GPRC5D, das auf bestimmten Tumorzellen wie z.B. dem Multiplen Myelom vermehrt vorkommt und eine Schlüsselrolle bei der Vermehrung von Tumorzellen spielt.
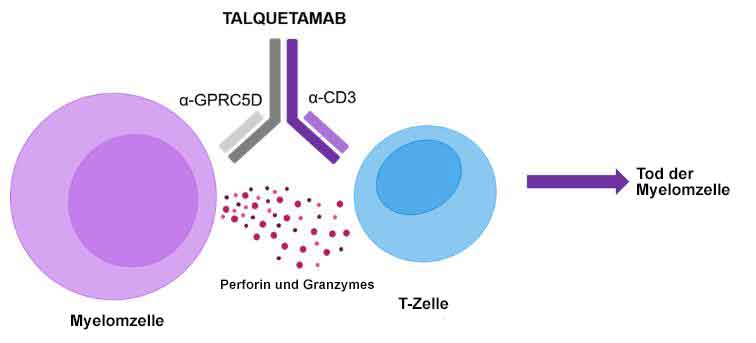
Abb. aus https://multiplemyelomahub.com/,
Teclistamab (JNJ-7957) ist ein bispezifischer Antikörper, der sowohl gegen BCMA als auch gegen CD3 gerichtet ist. BCMA ist ein Zelloberflächenprotein, das besonders auf Myelom- und Plasmazellen vorkommt und eine besondere biologische Bedeutung für das Überleben der Plasmazelle hat. Es wird bei Menschen mit Multiplem Myelom in signifikant höherem Maße exprimiert. CD3 ist an der Aktivierung der Immunantwort zur Bekämpfung von Infektionen beteiligt, Teclistamab lenkt CD3-T-Zellen auf BCMA-exprimierende Myelomzellen um, um die Zytotoxizität der Zielzellen zu induzieren. Ergebnisse aus präklinischen Studien zeigen, dass Teclistamab Myelom-Zelllinien und Myelom-Knochenmarkzellen von stark vorbehandelten Patienten abtötet.
Diese Studie geht davon aus, dass Talquetamab oder Teclistamab in Kombination mit einem PD-1-Inhibitor bei der Behandlung von rezidiviertem oder refraktärem Multiplem Myelom zu einem verbesserten klinischen Ansprechen führen, was auf verschiedene Wirkmechanismen zurückzuführen ist.
Einschlusskriterien:
- Dokumentierte Erstdiagnose eines Multiplen Myeloms nach den Diagnosekriterien der Internationalen Myelom-Arbeitsgruppe (IMWG)
- Teilnehmer mit rezidivierender oder refraktärer Erkrankung, die nicht für eine verfügbare Therapie mit nachgewiesenem klinischen Nutzen infrage kommen.
- Messbare Erkrankung zum Zeitpunkt des Screenings
- ECOG (Index zur Abstufung der Lebensqualität von Patienten mit Krebserkrankungen) von 0 oder 1
Ausschlusskriterien:
-
Vorangegangene Antitumortherapie innerhalb von 21 Tagen vor der ersten Dosis der Studienbehandlung (Therapie mit Proteasom-Inhibitoren [PI] oder Strahlentherapie innerhalb von 14 Tagen, Therapie mit immunmodulatorischen Wirkstoffen (IMiD) innerhalb von 7 Tagen, genmodifizierte adoptive Zelltherapie oder autologe Stammzelltransplantation innerhalb von 3 Monaten)
-
Vorherige Therapie mit PD-1-Inhibitoren, allogene Stammzelltransplantation oder Organtransplantation
-
Aktive Plasmazellleukämie, Waldenstrom-Makroglobulinämie, POEMS-Syndrom (Polyneuropathie, Organomegalie, Endokrinopathie, M-Protein und Hautveränderungen) oder primäre Leichtkettenamyloidose
-
Aktive Beteiligung des zentralen Nervensystems (ZNS) oder klinische Anzeichen einer meningealen Beteiligung des Multiplen Myeloms. Bei Verdacht auf eine der beiden Erkrankungen sind eine Magnetresonanztomographie des Gehirns (MRT) und eine Lumbalzytologie erforderlich.
-
Impfung mit einem abgeschwächten Lebendimpfstoff innerhalb von 4 Wochen vor der ersten Dosis der Studienbehandlung
Alle weiteren Kritereien besprechen Sie mit Ihrem Arzt
