COM_STUDIES_DEFAULT_PAGE_TITLE
Bayern
Aschaffenburg
Klinikum Aschaffenburg, Med. Klinik II
06021-32-0
Onkologie Aschaffenburg Dr. Welslau
06021-4527300
Studienzentrum Aschaffenburg
06021-3427-80
Augsburg
Hämatologische Onkologische Gemeinschaftspraxis Dr. Brudler, Dr. Heinrich, Dr. Bangerter
0821-34465-0
Klinikum Augsburg, II. Medizinische Klinik
Frau Söllner, 0821-400-3716
Studien
AlloRelapseMM
Allogene Stammzelltransplantation im Vergleich zur konventionellen Therapie als Salvage-Therapie für Patienten mit rezidiviertem / progredientem Multiplen Myelom nach einer Erstlinientherapie (AlloRelapseMMStudy)
Organisatorische Daten:
| Prüfplancode: | |
| ISRCTN: | |
| EudraCT: | 2021-001--5-67 |
| Clinicaltrials.gov: | NCT0567319 |
| DRKS: | |
| Sponsor: | Universitätsklinikum Hamburg-Eppendorf mit Unterstützung des Gemeinsamen Bundesausschusses (G-BA) |
| Studienphase: | III |
| Status: | Rekrutierung läuft, geplant bis 6/2027 |
Ziel:
In dieser Studie wird untersucht, ob die Transplantation von gespendeten Stammzellen (allogene Stammzelltransplantation) Vorteile gegenüber der gängigen Therapie bei Patienten mit Multiplem Myelom bietet, bei denen es nach einer Transplantation von körpereigenen Stammzellen (autologe Stammzelltransplantation) als Erstlinientherapie zu einem Erkrankungsrückfall (Rezidiv) oder einem Fortschreiten der Krankheit (Progression) gekommen ist. Es wird geprüft, ob die allogene Stammzelltransplantation das Gesamtüberleben bei diesen Patienten verlängert.
Hintergrund:
Eine Behandlungsoption des Multiplen Myeloms ist die Stammzelltransplantation. Nach einer Chemotherapie, bei der die Krebszellen zerstört werden, werden körpereigene (autologe) oder gespendete körperfremde (allogene) Stammzellen übertragen. Die übertragenen Stammzellen siedeln sich dann im Knochenmark an und bilden „frische“ Blutzellen. Die Stammzelltransplantation kommt als Behandlungsoption nach der ersten Diagnose (Erstlinientherapie), aber auch bei einem Rückfall nach Vorbehandlung (jenseits der Erstlinientherapie) in Frage. Auch wenn das Multiple Myelom oft nicht endgültig heilbar ist, soll die Therapie die Lebenserwartung verlängern und die Symptome zurückdrängen. (Quelle: https://www.g-ba.de/studien/erprobung/allorelapsemmstudy-studie/)
Ein- und Ausschlusskriterien (Auswahl):
Einschlusskriterien:
- Diagnose Multiples Myelom,
- Rückfall (Rezidiv) oder Fortschreiten (Progress) des Multiplen Myeloms unter oder nach einer autologen Stammzelltransplantation
- Erhalt von höchstens 1 Zyklus einer sogenannten Salvage-Therapie (Rezidiv-Therapie) vor Einschluss in die Studie
Ausschlusskriterien:
- Unzureichende Organfunktion gemäß der Definition im Prüfplan
- Aktive Hepatitis B oder C oder unkontrollierte HIV-Infektion
- Andere aktive bösartige Erkrankung
- Vorherige Behandlung mit allogenen Stammzellen
Alle weiteren Kriterien besprechen Sie bitte mit Ihrem behandelnden Arzt.
Onkologische Praxis, Herr Dr. med. Dirk Hempel, Internist und Onkologe
08237-959690
Bamberg
Klinikum Bamberg, Sozialstiftung Bamberg Klinikum am Bruderwald, Medizinische Klinik V
Studiensekretariat, 0951-503-13713
Bayreuth
Klinikum Bayreuth GmbH
Studiensekretariat, 0921-400-6350
Studien
GMMG-HD8/DSMM-XIX
Induktionstherapie mit Lenalidomid, Bortezomib und Dexamethason und entweder intravenösem oder subkutanem Isatuximab bei Patienten mit neu diagnostiziertem Multiplem Myelom, die für eine Hochdosis-Chemotherapie mit nachfolgender autologer Stammzelltransplantation geeignet sind
Organisatorische Daten:
| Prüfplancode: | GMMG-HD 8 / DSMM XIX |
| ISRCTN: | |
| EudraCT: | 2022-000996-38 |
| Clinicaltrials.gov: | NCT05804032 |
| DRKS: | |
| Sponsor: | Universitätsklinikum Heidelberg DSMM, Sanofi und KKS-Netzwerk |
| Studienphase: | |
| Status: | Rekrutierung geplant bis Juni 2025 |
Ziel:
In dieser Studie für Patienten mit zuvor unbehandeltem Multiplem Myelom soll die Wirksamkeit der Induktionstherapie mit Isatuximab in Kombination mit Lenalidomid/Bortezomib/Dexamethason (RVd) bei Gabe von Isatuximab unter die Haut (subkutan) gegenüber einer Gabe in die Vene (intravenös) untersucht werden.
Durchführung:
Randomisierung: Die Patienten werden vor der Induktionstherapie nach dem Zufallsverfahren (randomisiert) einem von 2 Studienarmen (A oder B) zugeordnet.
- Patienten in Arm A erhalten 3 Zyklen des monoklonalen Antikörpers Isatuximab intravenös in Kombination mit dem RVd-Schema (Lenalidomid, Bortezomib, Dexamethason). Jeder Zyklus hat eine Dauer von 42 Tagen.
- Patienten in Arm B erhalten 3 Zyklen Isatuximab subkutan in Kombination mit RVd.
Nach der Induktionstherapie erhalten die Patienten eine Standard-Intensivierung (in der Regel eine Mobilisierungstherapie auf Cyclophosphamid-Basis, Stammzellenentnahme und hochdosiertes Melphalan, gefolgt von einer autologen Stammzelltransplantation
Ein- und Ausschlusskriterien (Auswahl):
Einschlusskriterien:
- Bestätigte Diagnose eines neu diagnostizierten behandlungsbedürftigen Multiplen Myeloms gemäß den überarbeiteten Diagnosekriterien der International Myeloma Working Group (IMWG))
- Der Patient ist für eine Hochdosis-Chemotherapie und eine autologe Stammzelltransplantation geeignet
- Messbare Krankheitsaktivität (gemäß der Definition im Prüfplan)
- Alter 18 bis 70 Jahre bei Studieneinschluss
Ausschlußkriterien:
- Bekannte Überempfindlichkeit (oder Kontraindikation) gegen einen der Bestandteile der Studientherapie
- Systemische Amyloid-Leichtketten-Amyloidose (außer lokalisierte Amyloid-Leichtketten -Amyloidose, die auf die Haut oder das Knochenmark beschränkt ist)
- Plasmazell-Leukämie
- Vorherige Chemo- oder Strahlentherapie in den letzten 5 Jahren (außer lokaler Strahlentherapie bei lokalem Fortschreiten des Myeloms)
Alle weiteren Kriterien besprechen Sie bitte mit Ihrem behandelnden Arzt.
Coburg
Klinikum Coburg, Hämatologie und internistische Onkologie
09561-22-5413
Erlangen
Universitätsklinikum Erlangen
09131-85-0
Studien
CC-93269Studie zu CC-93269, einem BCMA x CD3 T-Zell-aktivierendem Antikörper, bei Patienten mit rezidivierendem und refraktärem multiplem Myelom
Organisatorische Daten:
| Prüfplancode: |
CC-93269 |
| ISRCTN: | |
| EudraCT: | |
| Clinicaltrials.gov: | NCT03486067 |
| DRKS: | |
| Sponsor: | Celgene |
| Studienphase: | Phase 1 |
| Status: | Rekrutierung läuft, geplant bis Juli 2027 |
Kurzbeschreibung:
In der offenen Phase-1-Studie CC-93269-MM-001 wird CC-93269 erstmals beim Menschen – und zwar bei Patienten mit rezidiviertem und refraktärem multiplem Myelom – untersucht.
Hintergrund:
CC-93269 ist ein sogenannter bispezifischer T-Zell Antikörper (BiTE Antikörper= Bi-specific T-cell engagers). Diese Antikörper verknüpfen das auf Myelomzellen vorhandene B-Zell-Reifungsantigen (BCMA) mit T-Zellen und führen so zu einer T-Zell vermittelten Zerstörung von Myelomzellen. BCMA, ein Mitglied der Tumornekrosefaktor-Rezeptor-Superfamilie, das auf malignen Plasmazellen vermehrt vertreten ist, spielt eine Schlüsselrolle bei der Förderung des Überlebens von Plasmazellen.
Durchführung:
Die Studie besteht aus zwei Teilen: einem Dosissteigerungsteil (Teil A) und einem Erweiterungsteil (Teil B). In Teil A wird die Sicherheit und Verträglichkeit von intravenös verabreichtem CC-93269 in steigenden Dosen bewertet, um die höchste verträgliche Dosis und die nicht verträgliche Dosis sowohl der ersten als auch der nachfolgenden Gaben von CC-93269 zu bestimmen. In Teil B wird die Sicherheit und Wirksamkeit von CC-93269, das den Teilnehmern in ausgewählten Studiengruppen in der höchsten verträglichen oder einer niedrigeren Dosis verabreicht wird, weiter untersucht, um die empfohlene Dosis für die Phase 2 zu bestimmen. Alle Behandlungen werden in 28-Tage-Zyklen bis zu 2 Jahre lang verabreicht, bis die Erkrankung fortschreitet, nicht vertretbare Nebenwirkungen auftreten oder der Teilnehmer/Prüfer sich zum Abbruch der Teilnahme entscheiden.
Einschlusskriterien:
- Multiples Myelom (MM) in der Vorgeschichte mit rezidivierter und refraktärer Erkrankung und erfolglose Behandlung mit, Unverträglichkeit gegenüber oder fehlende Eignung für verfügbare(n) Therapien
-
Messbare Krankheit gemäß Beurteilung durch ein Zentrallabor
-
Einwilligung zum Krankenhausaufenthalt zur Überwachung und zur Entnahme von peripheren Blutproben
-
Einwilligung zu Knochenmarkpunktionen und/oder Gewebeproben im Rahmen der Studie
Ausschlusskriterien:
- Vorbehandlung mit einer in der Erforschung befindlichen Therapie gegen das B-Zell-Reifungsantigen (BCMA)
- Multiples Myelom mit symptomatischer Beteiligung des zentralen Nervensystems
- Nicht-sezernierendes multiples Myelom, Plasmazellleukämie, Morbus Waldenström (Makroglobulinämie), POEMS-Syndrom (Polyneuropathie, Organomegalie, Endokrinopathie, monoklonales Protein und Hautveränderungen) oder Amyloidose
Alle weiteren Kriterien besprechen Sie bitte mit Ihrem behandelnden Arzt
TCR-Immuntherapie mit MDG1011
Erste Phase-1/2-Studie mit TCR-Immuntherapie MDG1011 am Menschen.
Diese Dosisfindungsstudie bewertet die Sicherheit, Durchführbarkeit und vorläufige Wirksamkeit von genmodifizierten T-Zellen bei Patienten mit myeloischen und lymphatischen Neoplasien, die mit einem hohen Risiko einhergehen.
Im Phase-1-Teil dieser multizentrischen, offenen klinischen Phase-1/2-Studie sollen ca. 12 Patienten behandelt werden, die HLA-A*02:01-positiv sind und an fortgeschrittenen hämatologischen Erkrankungen wie akuter myeloischer Leukämie (AML), myelodysplastischem Syndrom (MDS) oder multiplem Myelom (MM) leiden. Die Expression von PRAME ist eine weitere Voraussetzung zur Teilnahme an dieser Dosis-Eskalations-Studie. PRAME ist ein Krebs-Antigen, welches den Zelltod und die Zelldifferenzierung hemmt und vermutlich an der malignen Entartung beteiligt ist.
In drei Dosiskohorten und einer optionalen vierten Dosiskohorte werden Dosisbereiche von 100.000 bis 10.000.000 transduzierten (gen-modifizierten) T-Zellen pro kg Körpergewicht getestet. Jede Dosiskohorte wird je einen Patienten aus jeder der drei hämatologischen Erkrankungen enthalten. Die Patienten werden eine Vorbehandlung mit Cyclophosphamid und Fludarabin erhalten. Nach der vollständigen Behandlung aller Patienten einer Dosiskohorte und einer vierwöchigen Beobachtungsperiode zur Sicherheit wird ein unabhängiges "Data Safety and Monitoring Board" (DSMB) über den Start der nächsten Dosisgruppe entscheiden.
Organisatorische Daten:
| Prüfplancode: | CD-TCR-001 |
| ISRCTN: | |
| EudraCT: | 2017-000440-18 |
| Clinicaltrials.gov: | NCT03503968 |
| DRKS: | |
| Sponsor: | Medigene AG |
| Studienphase: | 1/2 |
| Status: | Rekrutierung läuft, geplant bis August 2020 |
Ziel:
Die primären Endpunkte für den Phase-1-Teil der klinischen Studie sind Sicherheit und Verträglichkeit von MDG1011, die maximal verträgliche Dosis und die für die Phase 2 empfohlene Dosis sowie die Durchführbarkeit. Als weitere Endpunkte werden die Gesamtansprechrate, die Dauer des Ansprechens, die Zeit bis zur Krankheitsprogression, das progressionsfreie Überleben, das Gesamtüberleben, die Lebensqualität und der Zusammenhang zwischen der PRAME-Expression mit der Antitumor-Antwort nach drei Monaten beurteilt. Insgesamt beträgt die Nachbeobachtungszeit bis zu 12 Monate.
Die Endpunkte des Phase-2-Teils sind die weitere Bewertung der Sicherheit und Wirksamkeit, wobei die Wirksamkeit als Gesamtansprechrate nach 3 Monaten gemessen wird. Die Studie wird eine Nachbeobachtungszeit von bis zu 12 Monaten haben. Weitere Endpunkte umfassen die Dauer des Ansprechens, die Zeit bis zur Progression, das progressionsfreie Überleben, das Gesamtüberleben, die Lebensqualität, die Durchführbarkeit und den Zusammenhang der PRAME-Expression mit der Antitumor-Antwort.
Die experimentelle TCR-Therapie MDG1011 wird im Rahmen dieser Studie erstmals am Menschen geprüft.
Hintergrund:
Die TCR-Technologie zielt darauf ab, körpereigene T-Zellen des Patienten mit tumorspezifischen T-Zell-Rezeptoren auszustatten. Die bezüglich ihres Rezeptors modifizierten T-Zellen sind dadurch in der Lage, Tumorzellen zu erkennen und wirksam zu zerstören. Dieser immuntherapeutische Ansatz versucht, die bestehende Toleranz gegenüber den Krebszellen und die tumor-induzierte Immunsuppression im Patienten zu überwinden, indem T-Zellen des Patienten außerhalb des Körpers aktiviert und modifiziert werden.
Ein- und Ausschlusskriterien (Auswahl):
Einschlusskriterien (allg.):
- Dokumentierte Diagnose der Erkrankung im letzten Stadium in den letzten 4 Wochen vor dem Screening
- Humanes Leukozytenantigen (HLA)
- Phase 1 und Phase 2 (Behandlungsgruppe): Nachweis von HLA-A*02:01
- Phase 2 (Vergleichsgruppe): kein Nachweis von HLA-A*02:01
- Lebenserwartung von mindestens 4 Monaten
- ECOG (Index zur Abstufung der Lebensqualität von Patienten mit Krebserkrankungen) von 0 bis 2
- keine geplante allogene hämatopoetische Stammzelltransplantation (HSZT)
Multiples Myelom-(MM-)spezifische Einschlusskriterien:
- Rezidiviertes und refraktäres MM
- Mindestens 3 vorangegangene Therapielinien mit mindestens einem Proteasomeninhibitor und einer immunmodulierenden Substanz (IMiD). Eine Induktion mit oder ohne hämatopoetische Stammzelltransplantation und mit oder ohne Erhaltungstherapie wird als ein einziges Behandlungsschema betrachtet.
- Myelomzellen müssen PRAME positiv exprimieren
Ausschlußkriterien:
- Akute Promyelozyten-Leukämiamit t(15;17)(q22;q12); Promyelozyten-Leukämia/Retinoic Acid Receptor Alpha (PML-RARA) oder mit varianten Translokationen
- Bekannter Nachweis des HIV-Virus, aktive Hepatitis-B-Virus-(HBV-) oder Hepatitis-C-Virus-(HCV-)Infektion
- Klinisch signifikante, fortgeschrittene oder instabile Erkrankung oder unzureichende Funktion eines Hauptorgans, die den Teilnehmer einem besonderen Risiko aussetzen könnte
- allogene Stammzelltransplantation in der Vorgeschichte
MM-spezifische Ausschlusskriterien für Phase 1 und Phase 2 (Behandlungsgruppe, falls das MM in Phase 2 fortschreitet):
- Vortherapie mit immunmodulierenden Substanzen (IMiDs) innerhalb von 14 Tagen vor der Leukapherese und/oder der Infusion des Prüfpräparats
- Vortherapie mit Kortikosteroiden innerhalb von 7 Tagen vor der Leukapherese oder 7 Tagen vor der Infusion des Prüfpräparats
Alle weiteren Kriterien besprechen Sie bitte mit Ihrem behandelnden Arzt.
Freising
Krankenhaus Freising GmbH
08161-24-3000
Fürth
Praxis Drs. Wilke/Wagner/Petzoldt
0911-979 22 23-0
Germering
Johann Mittermüller,Arzt für Innere Medizin Hämatologie und Internistische
089-842910
Hof
Hämatologisch-onkologische Praxis
09281-540060
Kempten
Klinikum Kempten, Hämatologie, Onkologie und Palliativmedizin
0831-530 2228
Studien
GMMG-HD8/DSMM-XIX
Induktionstherapie mit Lenalidomid, Bortezomib und Dexamethason und entweder intravenösem oder subkutanem Isatuximab bei Patienten mit neu diagnostiziertem Multiplem Myelom, die für eine Hochdosis-Chemotherapie mit nachfolgender autologer Stammzelltransplantation geeignet sind
Organisatorische Daten:
| Prüfplancode: | GMMG-HD 8 / DSMM XIX |
| ISRCTN: | |
| EudraCT: | 2022-000996-38 |
| Clinicaltrials.gov: | NCT05804032 |
| DRKS: | |
| Sponsor: | Universitätsklinikum Heidelberg DSMM, Sanofi und KKS-Netzwerk |
| Studienphase: | |
| Status: | Rekrutierung geplant bis Juni 2025 |
Ziel:
In dieser Studie für Patienten mit zuvor unbehandeltem Multiplem Myelom soll die Wirksamkeit der Induktionstherapie mit Isatuximab in Kombination mit Lenalidomid/Bortezomib/Dexamethason (RVd) bei Gabe von Isatuximab unter die Haut (subkutan) gegenüber einer Gabe in die Vene (intravenös) untersucht werden.
Durchführung:
Randomisierung: Die Patienten werden vor der Induktionstherapie nach dem Zufallsverfahren (randomisiert) einem von 2 Studienarmen (A oder B) zugeordnet.
- Patienten in Arm A erhalten 3 Zyklen des monoklonalen Antikörpers Isatuximab intravenös in Kombination mit dem RVd-Schema (Lenalidomid, Bortezomib, Dexamethason). Jeder Zyklus hat eine Dauer von 42 Tagen.
- Patienten in Arm B erhalten 3 Zyklen Isatuximab subkutan in Kombination mit RVd.
Nach der Induktionstherapie erhalten die Patienten eine Standard-Intensivierung (in der Regel eine Mobilisierungstherapie auf Cyclophosphamid-Basis, Stammzellenentnahme und hochdosiertes Melphalan, gefolgt von einer autologen Stammzelltransplantation
Ein- und Ausschlusskriterien (Auswahl):
Einschlusskriterien:
- Bestätigte Diagnose eines neu diagnostizierten behandlungsbedürftigen Multiplen Myeloms gemäß den überarbeiteten Diagnosekriterien der International Myeloma Working Group (IMWG))
- Der Patient ist für eine Hochdosis-Chemotherapie und eine autologe Stammzelltransplantation geeignet
- Messbare Krankheitsaktivität (gemäß der Definition im Prüfplan)
- Alter 18 bis 70 Jahre bei Studieneinschluss
Ausschlußkriterien:
- Bekannte Überempfindlichkeit (oder Kontraindikation) gegen einen der Bestandteile der Studientherapie
- Systemische Amyloid-Leichtketten-Amyloidose (außer lokalisierte Amyloid-Leichtketten -Amyloidose, die auf die Haut oder das Knochenmark beschränkt ist)
- Plasmazell-Leukämie
- Vorherige Chemo- oder Strahlentherapie in den letzten 5 Jahren (außer lokaler Strahlentherapie bei lokalem Fortschreiten des Myeloms)
Alle weiteren Kriterien besprechen Sie bitte mit Ihrem behandelnden Arzt.
Landshut
Klinikum Landshut
0871-698-0
München
Hämato-Onkologische Gemeinschaftspraxis Pasing
089 - 82 99 660
LMU - Medizinische Klinik und Poliklinik III der Universität München, Medizinische Klinik und Poliklinik III, Campus-Großhadern
089-4400-0
Studien
Cartitude 5Eine Studie zur Untersuchung von Bortezomib, Lenalidomid und Dexamethason (VRd) gefolgt von Ciltacabtagen-Autoleucel (Cilta-Cel, JNJ-68284528) im Vergleich zu VRd, gefolgt von Lenalidomid und Dexamethason (Rd) bei Teilnehmern mit neu diagnostiziertem Multiplem Myelom (MM), für die eine autologe Stammzelltransplantation (SZT) als Ersttherapie nicht vorgesehen ist (CARTITUDE-5)
Organisatorische Daten:
| Prüfplancode: | CARTITUDE-5 (68284528MMY3004, CR109015) |
| ISRCTN: | |
| EudraCT: | 2021-001242-35 |
| Clinicaltrials.gov: | NCT04923893 |
| DRKS: | |
| Sponsor: | Janssen |
| Studienphase: | III |
| Status: | Rekrutierung geplant bis Juni 2026 |
Ziel:
Die Studie soll untersuchen, ob die Behandlung mit VRd-Induktion gefolgt von einer einmaligen Verabreichung von Cilta-Cel im Vergleich zur Induktion mit Bortezomib, Lenalidomid und Dexamethason (VRd) und anschließender Rd-Erhaltung bei Teilnehmern mit neu diagnostiziertem MM das progressionsfreie Überleben signifikant verbessert.
Hintergrund:
Chimäre Antigenrezeptor-T-Zellen (CAR-T-Zellen) sind ein innovativer Ansatz zur Ausrottung von Krebszellen, bei dem die Kraft des patienteneigenen Immunsystems genutzt wird.
Bei Ciltacabtage-Autoleucel (Cilta-Cel; JNJ-68284528) handelt es sich um eine autologe CAR-T-Therapie, die auf das B-Zell-Reifungsantigen (BCMA) abzielt. Dieses Molekül kommt auf der Oberfläche von reifen B-Lymphozyten und bösartigen Plasmazellen vor. Indem Cilta-Cel gezielt gegen BCMA gerichtet ist, kann es Krebszellen vernichten, während gesunde Zellen unversehrt bleiben.
Durchführung:
Im Rahmen der Studie werden Teilnehmer mit neu diagnostiziertem MM untersucht, bei denen eine autologe Stammzelltransplantation (ASZT) als Ersttherapie nicht vorgesehen ist. Diese Studie wird in 4 Phasen durchgeführt: Screening (bis zu 28 Tage), Behandlung vor der Randomisierung, Behandlung und Nachbeobachtung.
Während der Studie werden verschiedene Untersuchungen zur Wirksamkeit und Sicherheit durchgeführt. Die Sicherheitsdaten werden in regelmäßigen Abständen von einem unabhängigen Datenüberwachungsausschuss überprüft. Die Dauer der Studie beträgt etwa 12 Jahre und 5 Monate.
Ablauf der Studie:

Ein- und Ausschlusskriterien (Auswahl):
Einschlusskriterien:
- Dokumentierte Diagnose eines Multiplen Myeloms (MM) gemäß den Diagnosekriterien der International Myeloma Working Group (IMWG)
- Messbare Erkrankung zum Zeitpunkt des Screenings, wie im Prüfplan definiert
- ECOG Performance Status (Index zur Abstufung der Lebensqualität von Patienten mit Krebserkrankungen) von 0 oder 1.
- Patient kommt nicht für eine Hochdosis-Chemotherapie mit autologer Stammzelltransplantation (ASCT) infrage
Ausschlußkriterien:
- Gebrechlichkeitsindex ≥ 2 gemäß dem Myeloma Geriatric Assessment Score (Index zur Abstufung der Gebrechlichkeit von Patienten von 0 bis 5, http://www.myelomafrailtyscorecalculator.net/)
- Periphere Neuropathie oder neuropathischer Schmerz Grad 2 oder höher (gemäß der Definition des National Cancer Institute-Common Terminology Criteria for Adverse Events (NCI-CTCAE) Version 5)
- Bekannte aktive oder frühere Beteiligung des zentralen Nervensystems (ZNS) oder klinische Anzeichen einer meningealen Beteiligung des MM
- Schlaganfall oder Krampfanfall innerhalb von 6 Monaten nach Unterzeichnung der Einwilligungserklärung
Alle weiteren Kriterien besprechen Sie bitte mit Ihrem behandelnden Arzt.
Belantamab-Mafodotin
Bewertung der Wirksamkeit und Sicherheit von Belantamab-Mafodotin, Bortezomib und Dexamethason gegenüber Daratumumab, Bortezomib und Dexamethason bei Teilnehmern mit rezidiviertem/refraktärem Multiplen Myelom
Organisatorische Daten:
| Prüfplancode: | 207503 |
| ISRCTN: | |
| EudraCT: | 2018-003993-29 |
| Clinicaltrials.gov: | NCT04246047 |
| DRKS: | |
| Sponsor: | GlaxoSmithKline |
| Studienphase: | III |
| Status: | Rekrutierung geplant bis Juni/2026 |
Kurzbeschreibung:
Hierbei handelt es sich um eine randomisierte, offene Phase-3-Studie zur Untersuchung der Sicherheit und Wirksamkeit von Belantamab-Mafodotin in Kombination mit Bortezomib/Dexamethason (Arm A) gegenüber Daratumumab in Kombination mit Bortezomib/Dexamethason (Arm B) bei Teilnehmern mit rezidivierendem multiplem Myelom..
Hintergrund:
Die amerikanische Arzneimittelbehörde FDA hat Belantamab-Mafodotin-blmf (GSK2857916; Blenrep) für die Behandlung von Patienten mit rezidiviertem oder refraktärem Multiplen Myelom zugelassen, die zuvor mit mindestens 4 Therapien behandelt wurden, darunter ein immunmodulatorisches Mittel, ein Proteasom-Inhibitor und ein Anti-CD38-Antikörper. Dies ist weltweit die erste Anti-BCMA-Behandlung, die bei dieser Patientenpopulation verfügbar ist.
Belantamab-Mafodotin ist gegen das B-Zell-Reifungsantigen (BCMA) gerichtet, das eine wichtige Rolle für das Überleben von Plasmazellen spielt und auf Zellen des Multiplen Myeloms exprimiert wird. Das Antikörper-Wirkstoff-Konjugat Belantamab-Mafodotin bindet an BCMA auf Myelom-Zelloberflächen, wodurch der Zellzyklus angehalten und eine antikörperabhängige zelluläre Zytotoxizität induziert wird.
Normalerweise fördert BCMA das Überleben von Plasmazellen durch Signalübertragung von zwei bekannten Liganden. Dieser Signalweg hat sich als wichtig für das Wachstum und Überleben von Myelomzellen erwiesen.
Ein- und Ausschlusskriterien (Auswahl):
Einschlusskriterien:
- Bestätigte Diagnose eines Multiplen Myeloms (MM) gemäß IMWG-Kriterien
- Vorbehandlung des MM mit mindestens einer Therapielinie und dokumentierte Krankheitsprogression während oder nach der letzten Therapie.
- ECOG Performance Status (Index zur Abstufung der Lebensqualität von Patienten mit Krebserkrankungen) von 0 bis 2
- Muss mindestens 1 Aspekt einer messbaren Erkrankung aufweisen, wie folgt definiert:
- Urin-M-Protein-Ausscheidung > 200 mg pro 24 Stunden, oder
- Serum-M-Protein-Konzentration > 0,5 g/dl, oder
- Freie Leichtketten im Serum (FLC): beteiligter FLC-Spiegel > 10 mg/dl (> 100 mg/L) und ein abnormes Verhältnis der freien Leichtketten im Serum (< 0,26 oder > 1,65).
- Alle Nebenwirkungen, die infolge durch Vorbehandlungen hervorgerufen wurden, müssen zum Zeitpunkt der Rekrutierung < Grad 1 sein, mit Ausnahme von Alopezie.
Ausschlußkriterien:
- Unverträglichkeit gegenüber Daratumumab.
- Kein bzw. kein hinreichendes Ansprechen (therapierefraktär) gegenüber Daratumumab oder einer anderen Anti-CD38-Therapie (definiert als fortschreitende Erkrankung während der Behandlung mit einer Anti-CD38-Therapie oder innerhalb von 60 Tagen nach Abschluss dieser Behandlung).
- Unverträglichkeit gegenüber Bortezomib oder kein bzw. kein hinreichendes Ansprechen (therapierefraktär) gegenüber Bortezomib (definiert als fortschreitende Erkrankung während der Behandlung mit einem Bortezomib-haltigen Schema von 1,3 mg/m2 zweimal wöchentlich oder innerhalb von 60 Tagen nach Abschluss dieser Behandlung). Hinweis: Patienten mit fortschreitender Erkrankung während der Behandlung mit einem wöchentlichen Bortezomib-Schema dürfen teilnehmen.
- Anhaltende periphere Neuropathie von Grad 2 oder höher oder neuropathische Schmerzen.
- Vorherige Behandlung mit einer Anti-B-Zellreifungsantigen- (Anti-BCMA-) Therapie.
Alle weiteren Kriterien besprechen Sie bitte mit Ihrem behandelnden Arzt.
Zusätzliche Information
Myelomsprechstunde
jeweils Dienstags, 08:00 - 16:00 Uhr
Tel: 089 - 4400-73041
MRI - III. Medizinische Klinik und Poliklinik der Technischen Universität Rechts der Isar
Prof. Dr. Florian Bassermann, 089 - 4140-5834
Studien
CC-92480Ein neuer Cereblon E3 Ligase Modulator
Eine Studie zur Bestimmung der empfohlenen Dosis und des Regimes und zur Bewertung der Sicherheit und vorläufigen Wirksamkeit von CC-92480 in Kombination mit Standardbehandlungen bei Patienten mit rezidiviertem oder refraktärem Multiplen Myelom (RRMM) und neu diagnostiziertem Multiplen Myelom (NDMM)
Organisatorische Daten:
| Prüfplancode: |
CC-92480-mm-02 |
| UTMS | U1111-1233-5619 |
| EudraCT: | 2018-004767-31 |
| Clinicaltrials.gov: | NCT03989414 |
| DRKS: | |
| Sponsor: | Celgene |
| Studienphase: | Phase 1/2 |
| Status: | Rekrutierung läuft, geplant bis Januar 2025 |
Hintergrund:
CC-92480 ist ein sogenannter CRBN-Modulator [Cereblon-(CRBN-)E3-Ligase-Modulator (CELMoD)]. Dieser neuartige Modulator hat vielfältige Wirkungen und wirkt unter anderem stark immunmodulierend. Der Wirkstoff führt zu einem schnellen, tiefen und anhaltenden Zerfall von Ikaros und Aiolos – zwei Faktoren, die zum Überleben der Myelomzellen beitragen.
Durchführung:
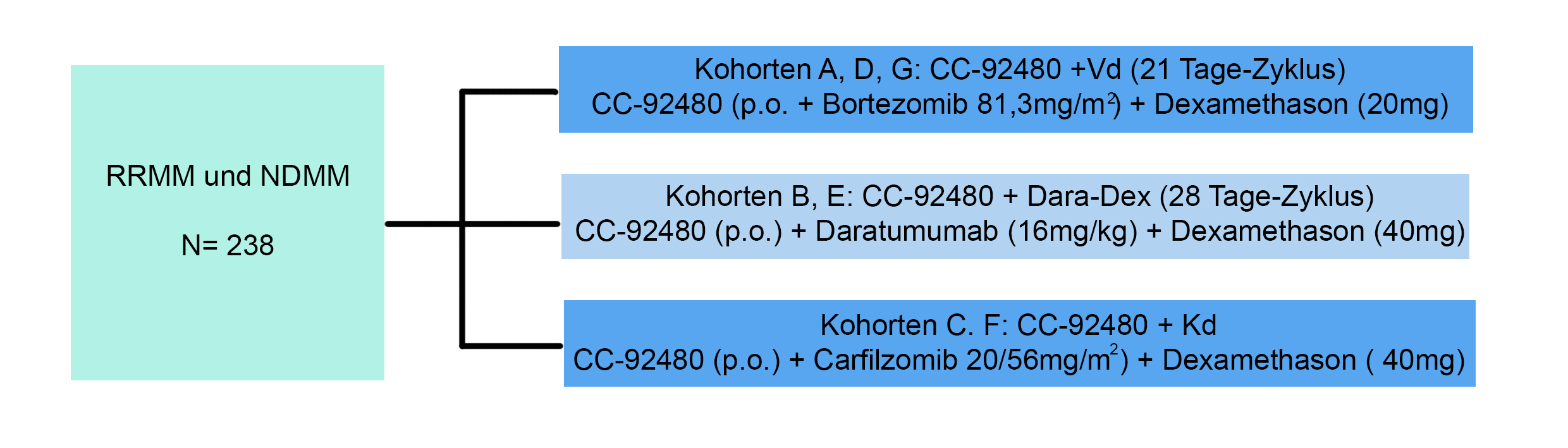
Die Studie wird randomisiert ausgeführt und die Patienten in 3 Gruppen eingeteilt, die neben dem CC-92480 unterschiedliche Zweier-Kombinationen enthalten, die gegeneinander getestet werden. Die Kohorten haben unterschiedliche Einschlusskriterien.
Ein und Ausschlusskriterien:
Einschlusskriterien:
- Alter ≥ 18 Jahre alt und ECOG (Index zur Abstufung der Lebensqualität von Patienten mit Krebserkrankungen) mit 0, 1 oder 2 Punkten.
- Patienten mit rezidiviertem oder refraktäremMultiplen Myelom müssen eine messbare Krankheit haben und ihr Krankheitsverlauf während oder nach ihrer letzten Myelomtherapie muss dokumentiert sein.
- Bei neu diagnostizierten Patienten muss die Diagnose eines zuvor unbehandelten symptomatischen Multiplen Myeloms dokumentiert sein.
- Frauen im gebärfähigen Alter und männliche Patienten müssen mit dem Schwangerschaftsverhütungsplan einverstanden sein.
Ausschlusskriterien:
- Signifikante medizinische Erkrankung, auffällige Laborwerte oder eine psychiatrische Krankheit, die an der Teilnahme an der Studie hindert.
- Patient ist nicht in der Lage oder nicht bereit, sich der laut Prüfplan vorgeschriebenen Prophylaxe einer Thromboembolie zu unterziehen.
Alle weiteren Kriterien besprechen Sie bitte mit Ihrem behandelnden Arzt
Studie zu CC-93269, einem BCMA x CD3 T-Zell-aktivierendem Antikörper, bei Patienten mit rezidivierendem und refraktärem multiplem Myelom
Organisatorische Daten:
| Prüfplancode: |
CC-93269 |
| ISRCTN: | |
| EudraCT: | |
| Clinicaltrials.gov: | NCT03486067 |
| DRKS: | |
| Sponsor: | Celgene |
| Studienphase: | Phase 1 |
| Status: | Rekrutierung läuft, geplant bis Juli 2027 |
Kurzbeschreibung:
In der offenen Phase-1-Studie CC-93269-MM-001 wird CC-93269 erstmals beim Menschen – und zwar bei Patienten mit rezidiviertem und refraktärem multiplem Myelom – untersucht.
Hintergrund:
CC-93269 ist ein sogenannter bispezifischer T-Zell Antikörper (BiTE Antikörper= Bi-specific T-cell engagers). Diese Antikörper verknüpfen das auf Myelomzellen vorhandene B-Zell-Reifungsantigen (BCMA) mit T-Zellen und führen so zu einer T-Zell vermittelten Zerstörung von Myelomzellen. BCMA, ein Mitglied der Tumornekrosefaktor-Rezeptor-Superfamilie, das auf malignen Plasmazellen vermehrt vertreten ist, spielt eine Schlüsselrolle bei der Förderung des Überlebens von Plasmazellen.
Durchführung:
Die Studie besteht aus zwei Teilen: einem Dosissteigerungsteil (Teil A) und einem Erweiterungsteil (Teil B). In Teil A wird die Sicherheit und Verträglichkeit von intravenös verabreichtem CC-93269 in steigenden Dosen bewertet, um die höchste verträgliche Dosis und die nicht verträgliche Dosis sowohl der ersten als auch der nachfolgenden Gaben von CC-93269 zu bestimmen. In Teil B wird die Sicherheit und Wirksamkeit von CC-93269, das den Teilnehmern in ausgewählten Studiengruppen in der höchsten verträglichen oder einer niedrigeren Dosis verabreicht wird, weiter untersucht, um die empfohlene Dosis für die Phase 2 zu bestimmen. Alle Behandlungen werden in 28-Tage-Zyklen bis zu 2 Jahre lang verabreicht, bis die Erkrankung fortschreitet, nicht vertretbare Nebenwirkungen auftreten oder der Teilnehmer/Prüfer sich zum Abbruch der Teilnahme entscheiden.
Einschlusskriterien:
- Multiples Myelom (MM) in der Vorgeschichte mit rezidivierter und refraktärer Erkrankung und erfolglose Behandlung mit, Unverträglichkeit gegenüber oder fehlende Eignung für verfügbare(n) Therapien
-
Messbare Krankheit gemäß Beurteilung durch ein Zentrallabor
-
Einwilligung zum Krankenhausaufenthalt zur Überwachung und zur Entnahme von peripheren Blutproben
-
Einwilligung zu Knochenmarkpunktionen und/oder Gewebeproben im Rahmen der Studie
Ausschlusskriterien:
- Vorbehandlung mit einer in der Erforschung befindlichen Therapie gegen das B-Zell-Reifungsantigen (BCMA)
- Multiples Myelom mit symptomatischer Beteiligung des zentralen Nervensystems
- Nicht-sezernierendes multiples Myelom, Plasmazellleukämie, Morbus Waldenström (Makroglobulinämie), POEMS-Syndrom (Polyneuropathie, Organomegalie, Endokrinopathie, monoklonales Protein und Hautveränderungen) oder Amyloidose
Alle weiteren Kriterien besprechen Sie bitte mit Ihrem behandelnden Arzt
Induktionstherapie mit Lenalidomid, Bortezomib und Dexamethason und entweder intravenösem oder subkutanem Isatuximab bei Patienten mit neu diagnostiziertem Multiplem Myelom, die für eine Hochdosis-Chemotherapie mit nachfolgender autologer Stammzelltransplantation geeignet sind
Organisatorische Daten:
| Prüfplancode: | GMMG-HD 8 / DSMM XIX |
| ISRCTN: | |
| EudraCT: | 2022-000996-38 |
| Clinicaltrials.gov: | NCT05804032 |
| DRKS: | |
| Sponsor: | Universitätsklinikum Heidelberg DSMM, Sanofi und KKS-Netzwerk |
| Studienphase: | |
| Status: | Rekrutierung geplant bis Juni 2025 |
Ziel:
In dieser Studie für Patienten mit zuvor unbehandeltem Multiplem Myelom soll die Wirksamkeit der Induktionstherapie mit Isatuximab in Kombination mit Lenalidomid/Bortezomib/Dexamethason (RVd) bei Gabe von Isatuximab unter die Haut (subkutan) gegenüber einer Gabe in die Vene (intravenös) untersucht werden.
Durchführung:
Randomisierung: Die Patienten werden vor der Induktionstherapie nach dem Zufallsverfahren (randomisiert) einem von 2 Studienarmen (A oder B) zugeordnet.
- Patienten in Arm A erhalten 3 Zyklen des monoklonalen Antikörpers Isatuximab intravenös in Kombination mit dem RVd-Schema (Lenalidomid, Bortezomib, Dexamethason). Jeder Zyklus hat eine Dauer von 42 Tagen.
- Patienten in Arm B erhalten 3 Zyklen Isatuximab subkutan in Kombination mit RVd.
Nach der Induktionstherapie erhalten die Patienten eine Standard-Intensivierung (in der Regel eine Mobilisierungstherapie auf Cyclophosphamid-Basis, Stammzellenentnahme und hochdosiertes Melphalan, gefolgt von einer autologen Stammzelltransplantation
Ein- und Ausschlusskriterien (Auswahl):
Einschlusskriterien:
- Bestätigte Diagnose eines neu diagnostizierten behandlungsbedürftigen Multiplen Myeloms gemäß den überarbeiteten Diagnosekriterien der International Myeloma Working Group (IMWG))
- Der Patient ist für eine Hochdosis-Chemotherapie und eine autologe Stammzelltransplantation geeignet
- Messbare Krankheitsaktivität (gemäß der Definition im Prüfplan)
- Alter 18 bis 70 Jahre bei Studieneinschluss
Ausschlußkriterien:
- Bekannte Überempfindlichkeit (oder Kontraindikation) gegen einen der Bestandteile der Studientherapie
- Systemische Amyloid-Leichtketten-Amyloidose (außer lokalisierte Amyloid-Leichtketten -Amyloidose, die auf die Haut oder das Knochenmark beschränkt ist)
- Plasmazell-Leukämie
- Vorherige Chemo- oder Strahlentherapie in den letzten 5 Jahren (außer lokaler Strahlentherapie bei lokalem Fortschreiten des Myeloms)
Alle weiteren Kriterien besprechen Sie bitte mit Ihrem behandelnden Arzt.
Zusätzliche Information
Myelomsprechstunde
Terminvereinbarung unter Tel. 089 - 4140-4107
Onkologische Praxis Elisenhof
(089) 45 22 56-0
Onkologische Schwerpunktpraxis Dr. med. Walther
089-554417
Rotkreuzklinikum München Abteilung für Innere Medizin III – Hämatologie und Onkologie
(089) 1303-0
Studien
GMMG-HD8/DSMM-XIX
Induktionstherapie mit Lenalidomid, Bortezomib und Dexamethason und entweder intravenösem oder subkutanem Isatuximab bei Patienten mit neu diagnostiziertem Multiplem Myelom, die für eine Hochdosis-Chemotherapie mit nachfolgender autologer Stammzelltransplantation geeignet sind
Organisatorische Daten:
| Prüfplancode: | GMMG-HD 8 / DSMM XIX |
| ISRCTN: | |
| EudraCT: | 2022-000996-38 |
| Clinicaltrials.gov: | NCT05804032 |
| DRKS: | |
| Sponsor: | Universitätsklinikum Heidelberg DSMM, Sanofi und KKS-Netzwerk |
| Studienphase: | |
| Status: | Rekrutierung geplant bis Juni 2025 |
Ziel:
In dieser Studie für Patienten mit zuvor unbehandeltem Multiplem Myelom soll die Wirksamkeit der Induktionstherapie mit Isatuximab in Kombination mit Lenalidomid/Bortezomib/Dexamethason (RVd) bei Gabe von Isatuximab unter die Haut (subkutan) gegenüber einer Gabe in die Vene (intravenös) untersucht werden.
Durchführung:
Randomisierung: Die Patienten werden vor der Induktionstherapie nach dem Zufallsverfahren (randomisiert) einem von 2 Studienarmen (A oder B) zugeordnet.
- Patienten in Arm A erhalten 3 Zyklen des monoklonalen Antikörpers Isatuximab intravenös in Kombination mit dem RVd-Schema (Lenalidomid, Bortezomib, Dexamethason). Jeder Zyklus hat eine Dauer von 42 Tagen.
- Patienten in Arm B erhalten 3 Zyklen Isatuximab subkutan in Kombination mit RVd.
Nach der Induktionstherapie erhalten die Patienten eine Standard-Intensivierung (in der Regel eine Mobilisierungstherapie auf Cyclophosphamid-Basis, Stammzellenentnahme und hochdosiertes Melphalan, gefolgt von einer autologen Stammzelltransplantation
Ein- und Ausschlusskriterien (Auswahl):
Einschlusskriterien:
- Bestätigte Diagnose eines neu diagnostizierten behandlungsbedürftigen Multiplen Myeloms gemäß den überarbeiteten Diagnosekriterien der International Myeloma Working Group (IMWG))
- Der Patient ist für eine Hochdosis-Chemotherapie und eine autologe Stammzelltransplantation geeignet
- Messbare Krankheitsaktivität (gemäß der Definition im Prüfplan)
- Alter 18 bis 70 Jahre bei Studieneinschluss
Ausschlußkriterien:
- Bekannte Überempfindlichkeit (oder Kontraindikation) gegen einen der Bestandteile der Studientherapie
- Systemische Amyloid-Leichtketten-Amyloidose (außer lokalisierte Amyloid-Leichtketten -Amyloidose, die auf die Haut oder das Knochenmark beschränkt ist)
- Plasmazell-Leukämie
- Vorherige Chemo- oder Strahlentherapie in den letzten 5 Jahren (außer lokaler Strahlentherapie bei lokalem Fortschreiten des Myeloms)
Alle weiteren Kriterien besprechen Sie bitte mit Ihrem behandelnden Arzt.
Zusätzliche Information
Myelomsprechstunden:
Prof. Dr. Marcus Hentrich, Terminvereinbarung unter (089) 1303-4372 (Sekretariat)
PD Dr. med. Peter Bojko, Terminvereinbarung unter (089)1303-4372
Städtisches Klinikum München Schwabing, Klinik für Hämatologie, Onkologie, Immunologie, Palliativmedizin, Infektiologie und Tropenmedizin
(089) 3068-2228
Studien
DSMM XIVPhase III-Studie zum Vergleich einer Induktionstherapie aus Lenalidomid, Adriamycin, Dexamethason (RAD) mit Lenalidomid, Bortezomib, Dexamethason (VRD) gefolgt von einer am Ansprechen ausgerichteten Stammzelltransplantation bei Patienten mit neu diagnostiziertem multiplen Myelom.
| Prüfplancode: | DSMM XIV |
| ISRCTN: | |
| EudraCT: | 2009-016616-21 |
| Clincaltrials.gov: | NCT01685814 |
| DRKS: | 0003967 |
Allgemeine Informationen
In der Studie werden die Raten der kompletten Remission zweier Induktionsschemata (ein neues Medikament [RAD] gegen zwei neue Medikamente [VRD]) bei Patienten mit neu diagnostiziertem multiplem Myelom verglichen und das progressionsfreie Überleben nach einer Konsolidierungsbehandlung bestimmt.
Die Patienten sollten Über 18 Jahre und unter 65 Jahre alt sein, bisher ohne eine systemische Myelomtherapie sein und für eine Stammzelltransplantation in Frage kommen.
Die weiteren Ein- und Ausschlusskriterien kann man hier nachlesen.
Zusätzliche Information
Ärztliche Leitung
Prof. Dr. Clemens Wendtner
Prof. Dr. Christian Straka
Städtisches Krankenhaus München, Klinikum Harlaching, Abt. für Hämatologie, Onkologie und Palliativmedizin
(089) 6210-2731
Zusätzliche Information
Ärztliche Leitung:
Prof. Dr. Meinolf Karthaus
Neumarkt i.d.O.
Onkologische Schwerpunktpraxis Neumarkt, Innere Medizin
Dr. med. Ladda, 09181-464526
Nürnberg
Klinikum Nürnberg Nord, Medizinische klinik 5, Schwerpunkt Onkologie, Hämatologie
Prof. Dr. med. Hannes Wandt, 0911-398-3650
Hannes.Wandt@klinikum-nuernberg.de
Studien
Successor-2Studie zu CC-94260
Eine Studie zur Bewertung von CC-92480 in Kombination mit Carfilzomib und Dexamethason (480Kd) im Vergleich zu Carfilzomib und Dexamethason (Kd) bei Teilnehmern mit rezidiviertem oder refraktärem Multiplem Myelom (SUCCESSOR-2)
Organisatorische Daten:
| Prüfplancode: | CA057-008 |
| ISRCTN: | |
| EudraCT: | |
| Clinicaltrials.gov: | NCT05552976 |
| DRKS: | |
| Sponsor: | Bristol Meyer Squibb |
| Studienphase: | Phase 3 |
| Status: | Rekrutierung läuft, geplant bis Februar 2026 |
Ziele:
Ziel der Studie ist der Vergleich von CC-92480 (BMS-986348) mit Carfilzomib und Dexamethason (480Kd) gegen Carfilzomib und Dexamethason (Kd) bei der Behandlung von RRMM.
Hintergrund:
CC-92480 ist ein sogenannter CRBN-Modulator [Cereblon-(CRBN-)E3-Ligase-Modulator (CELMoD)]. Dieser neuartige Modulator hat vielfältige Wirkungen und wirkt unter anderem stark immunmodulierend. Der Wirkstoff führt zu einem schnellen, tiefen und anhaltenden Zerfall von Ikaros und Aiolos – zwei Faktoren, die zum Überleben der Myelomzellen beitragen.
Ein- und Ausschlusskriterien (Auswahl):
Einschlusskriterien:
- Der Teilnehmer hat eine dokumentierte Diagnose eines Multiplen Myeloms und eine messbare Erkrankung, gemäß der Definition im Protokoll.
- Der Teilnehmer hat mindestens eine vorherige Linie einer Myelom-Therapie erhalten. Hinweis: Eine Linie kann mehrere Phasen umfassen (z. B. Induktion, [mit oder ohne] hämatopoetische Stammzelltransplantation, (mit oder ohne) Konsolidierung und/oder [mit oder ohne] Erhaltungstherapie).
- Der Teilnehmer muss zuvor eine Behandlung mit Lenalidomid und einem monoklonalen Anti-CD38-Antikörper erhalten haben.
- Der Teilnehmer hat auf mindestens eine vorherige Myelom-Therapie minimal oder besser angesprochen.
- Bei dem Teilnehmer muss während oder nach seiner letzten Myelom-Therapie ein Fortschreiten der Erkrankung dokumentiert sein.
Ausschlusskriterien:
- Der Teilnehmer wurde zuvor mit CC-92480 oder Carfilzomib behandelt.
- Der Teilnehmer hat zu irgendeinem Zeitpunkt eine allogene Stammzelltransplantation oder innerhalb von 12 Wochen vor Beginn der Studienbehandlung eine autologe Stammzelltransplantation erhalten.
Alle weiteren Kriterien besprechen Sie bitte mit Ihrem behandelnden Arzt
Regensburg
Krankenhaus Barmherzige Brüder - Onkologisches Zentrum
Studien
GMMG-HD8/DSMM-XIX
Induktionstherapie mit Lenalidomid, Bortezomib und Dexamethason und entweder intravenösem oder subkutanem Isatuximab bei Patienten mit neu diagnostiziertem Multiplem Myelom, die für eine Hochdosis-Chemotherapie mit nachfolgender autologer Stammzelltransplantation geeignet sind
Organisatorische Daten:
| Prüfplancode: | GMMG-HD 8 / DSMM XIX |
| ISRCTN: | |
| EudraCT: | 2022-000996-38 |
| Clinicaltrials.gov: | NCT05804032 |
| DRKS: | |
| Sponsor: | Universitätsklinikum Heidelberg DSMM, Sanofi und KKS-Netzwerk |
| Studienphase: | |
| Status: | Rekrutierung geplant bis Juni 2025 |
Ziel:
In dieser Studie für Patienten mit zuvor unbehandeltem Multiplem Myelom soll die Wirksamkeit der Induktionstherapie mit Isatuximab in Kombination mit Lenalidomid/Bortezomib/Dexamethason (RVd) bei Gabe von Isatuximab unter die Haut (subkutan) gegenüber einer Gabe in die Vene (intravenös) untersucht werden.
Durchführung:
Randomisierung: Die Patienten werden vor der Induktionstherapie nach dem Zufallsverfahren (randomisiert) einem von 2 Studienarmen (A oder B) zugeordnet.
- Patienten in Arm A erhalten 3 Zyklen des monoklonalen Antikörpers Isatuximab intravenös in Kombination mit dem RVd-Schema (Lenalidomid, Bortezomib, Dexamethason). Jeder Zyklus hat eine Dauer von 42 Tagen.
- Patienten in Arm B erhalten 3 Zyklen Isatuximab subkutan in Kombination mit RVd.
Nach der Induktionstherapie erhalten die Patienten eine Standard-Intensivierung (in der Regel eine Mobilisierungstherapie auf Cyclophosphamid-Basis, Stammzellenentnahme und hochdosiertes Melphalan, gefolgt von einer autologen Stammzelltransplantation
Ein- und Ausschlusskriterien (Auswahl):
Einschlusskriterien:
- Bestätigte Diagnose eines neu diagnostizierten behandlungsbedürftigen Multiplen Myeloms gemäß den überarbeiteten Diagnosekriterien der International Myeloma Working Group (IMWG))
- Der Patient ist für eine Hochdosis-Chemotherapie und eine autologe Stammzelltransplantation geeignet
- Messbare Krankheitsaktivität (gemäß der Definition im Prüfplan)
- Alter 18 bis 70 Jahre bei Studieneinschluss
Ausschlußkriterien:
- Bekannte Überempfindlichkeit (oder Kontraindikation) gegen einen der Bestandteile der Studientherapie
- Systemische Amyloid-Leichtketten-Amyloidose (außer lokalisierte Amyloid-Leichtketten -Amyloidose, die auf die Haut oder das Knochenmark beschränkt ist)
- Plasmazell-Leukämie
- Vorherige Chemo- oder Strahlentherapie in den letzten 5 Jahren (außer lokaler Strahlentherapie bei lokalem Fortschreiten des Myeloms)
Alle weiteren Kriterien besprechen Sie bitte mit Ihrem behandelnden Arzt.
Universitätsklinikum Regensburg
0941-944-5541
Studien
CD-TCR-001TCR-Immuntherapie mit MDG1011
Erste Phase-1/2-Studie mit TCR-Immuntherapie MDG1011 am Menschen.
Diese Dosisfindungsstudie bewertet die Sicherheit, Durchführbarkeit und vorläufige Wirksamkeit von genmodifizierten T-Zellen bei Patienten mit myeloischen und lymphatischen Neoplasien, die mit einem hohen Risiko einhergehen.
Im Phase-1-Teil dieser multizentrischen, offenen klinischen Phase-1/2-Studie sollen ca. 12 Patienten behandelt werden, die HLA-A*02:01-positiv sind und an fortgeschrittenen hämatologischen Erkrankungen wie akuter myeloischer Leukämie (AML), myelodysplastischem Syndrom (MDS) oder multiplem Myelom (MM) leiden. Die Expression von PRAME ist eine weitere Voraussetzung zur Teilnahme an dieser Dosis-Eskalations-Studie. PRAME ist ein Krebs-Antigen, welches den Zelltod und die Zelldifferenzierung hemmt und vermutlich an der malignen Entartung beteiligt ist.
In drei Dosiskohorten und einer optionalen vierten Dosiskohorte werden Dosisbereiche von 100.000 bis 10.000.000 transduzierten (gen-modifizierten) T-Zellen pro kg Körpergewicht getestet. Jede Dosiskohorte wird je einen Patienten aus jeder der drei hämatologischen Erkrankungen enthalten. Die Patienten werden eine Vorbehandlung mit Cyclophosphamid und Fludarabin erhalten. Nach der vollständigen Behandlung aller Patienten einer Dosiskohorte und einer vierwöchigen Beobachtungsperiode zur Sicherheit wird ein unabhängiges "Data Safety and Monitoring Board" (DSMB) über den Start der nächsten Dosisgruppe entscheiden.
Organisatorische Daten:
| Prüfplancode: | CD-TCR-001 |
| ISRCTN: | |
| EudraCT: | 2017-000440-18 |
| Clinicaltrials.gov: | NCT03503968 |
| DRKS: | |
| Sponsor: | Medigene AG |
| Studienphase: | 1/2 |
| Status: | Rekrutierung läuft, geplant bis August 2020 |
Ziel:
Die primären Endpunkte für den Phase-1-Teil der klinischen Studie sind Sicherheit und Verträglichkeit von MDG1011, die maximal verträgliche Dosis und die für die Phase 2 empfohlene Dosis sowie die Durchführbarkeit. Als weitere Endpunkte werden die Gesamtansprechrate, die Dauer des Ansprechens, die Zeit bis zur Krankheitsprogression, das progressionsfreie Überleben, das Gesamtüberleben, die Lebensqualität und der Zusammenhang zwischen der PRAME-Expression mit der Antitumor-Antwort nach drei Monaten beurteilt. Insgesamt beträgt die Nachbeobachtungszeit bis zu 12 Monate.
Die Endpunkte des Phase-2-Teils sind die weitere Bewertung der Sicherheit und Wirksamkeit, wobei die Wirksamkeit als Gesamtansprechrate nach 3 Monaten gemessen wird. Die Studie wird eine Nachbeobachtungszeit von bis zu 12 Monaten haben. Weitere Endpunkte umfassen die Dauer des Ansprechens, die Zeit bis zur Progression, das progressionsfreie Überleben, das Gesamtüberleben, die Lebensqualität, die Durchführbarkeit und den Zusammenhang der PRAME-Expression mit der Antitumor-Antwort.
Die experimentelle TCR-Therapie MDG1011 wird im Rahmen dieser Studie erstmals am Menschen geprüft.
Hintergrund:
Die TCR-Technologie zielt darauf ab, körpereigene T-Zellen des Patienten mit tumorspezifischen T-Zell-Rezeptoren auszustatten. Die bezüglich ihres Rezeptors modifizierten T-Zellen sind dadurch in der Lage, Tumorzellen zu erkennen und wirksam zu zerstören. Dieser immuntherapeutische Ansatz versucht, die bestehende Toleranz gegenüber den Krebszellen und die tumor-induzierte Immunsuppression im Patienten zu überwinden, indem T-Zellen des Patienten außerhalb des Körpers aktiviert und modifiziert werden.
Ein- und Ausschlusskriterien (Auswahl):
Einschlusskriterien (allg.):
- Dokumentierte Diagnose der Erkrankung im letzten Stadium in den letzten 4 Wochen vor dem Screening
- Humanes Leukozytenantigen (HLA)
- Phase 1 und Phase 2 (Behandlungsgruppe): Nachweis von HLA-A*02:01
- Phase 2 (Vergleichsgruppe): kein Nachweis von HLA-A*02:01
- Lebenserwartung von mindestens 4 Monaten
- ECOG (Index zur Abstufung der Lebensqualität von Patienten mit Krebserkrankungen) von 0 bis 2
- keine geplante allogene hämatopoetische Stammzelltransplantation (HSZT)
Multiples Myelom-(MM-)spezifische Einschlusskriterien:
- Rezidiviertes und refraktäres MM
- Mindestens 3 vorangegangene Therapielinien mit mindestens einem Proteasomeninhibitor und einer immunmodulierenden Substanz (IMiD). Eine Induktion mit oder ohne hämatopoetische Stammzelltransplantation und mit oder ohne Erhaltungstherapie wird als ein einziges Behandlungsschema betrachtet.
- Myelomzellen müssen PRAME positiv exprimieren
Ausschlußkriterien:
- Akute Promyelozyten-Leukämiamit t(15;17)(q22;q12); Promyelozyten-Leukämia/Retinoic Acid Receptor Alpha (PML-RARA) oder mit varianten Translokationen
- Bekannter Nachweis des HIV-Virus, aktive Hepatitis-B-Virus-(HBV-) oder Hepatitis-C-Virus-(HCV-)Infektion
- Klinisch signifikante, fortgeschrittene oder instabile Erkrankung oder unzureichende Funktion eines Hauptorgans, die den Teilnehmer einem besonderen Risiko aussetzen könnte
- allogene Stammzelltransplantation in der Vorgeschichte
MM-spezifische Ausschlusskriterien für Phase 1 und Phase 2 (Behandlungsgruppe, falls das MM in Phase 2 fortschreitet):
- Vortherapie mit immunmodulierenden Substanzen (IMiDs) innerhalb von 14 Tagen vor der Leukapherese und/oder der Infusion des Prüfpräparats
- Vortherapie mit Kortikosteroiden innerhalb von 7 Tagen vor der Leukapherese oder 7 Tagen vor der Infusion des Prüfpräparats
Alle weiteren Kriterien besprechen Sie bitte mit Ihrem behandelnden Arzt.
Intravenös verabreichtes ABBV-383 in Kombination mit Krebstherapien bei Patienten mit rezidiviertem oder refraktärem Multiplen Myelom: eine Studie zur Bewertung der unerwünschten Ereignisse und der Veränderung der Krankheitsaktivität
Organisatorische Daten:
NCT05259839
| Prüfplancode: |
M22-947 |
| ISRCTN: | |
| EudraCT: | |
| Clinicaltrials.gov: | NCT05259839 |
| DRKS: | |
| Sponsor: | TeneoOne Inc |
| Studienphase: | Phase 1, Erstanwendung am Menschen |
| Status: | Rekrutierung läuft, geplant bis Okt.2028 |
Ziele:
Das Multiple Myelom (MM) ist eine Plasmazellerkrankung, die durch das Wachstum klonaler Plasmazellen im Knochenmark gekennzeichnet ist. Ziel dieser Studie ist es, die Sicherheit und Toxizität von ABBV-383 bei gleichzeitiger Verabreichung mit Pomalidomid-Dexamethason (Pd), Lenalidomid-Dexamethason (Rd), Daratumumab-Dexamethason (Dd) oder Nirogacestat (Niro) bei erwachsenen Teilnehmern mit rezidiviertem/refraktärem Multiplem Myelom (MM) zu untersuchen. Es werden unerwünschte Ereignisse und Veränderungen der Krankheitsaktivität bewertet.
Durchführung:
In dieser Studie werden die Teilnehmer in Gruppen eingeteilt, die als Behandlungsarme bezeichnet werden. Untersucht wird ABBV-383 in Kombination mit Pd, Rd, Dd oder Niro. Jeder Behandlungsarm erhält eine andere Behandlungskombination, je nach Stadium der Studie und Eignung des Teilnehmers. Die Studie umfasst eine Dosissteigerungsphase, in der die beste Dosis von ABB-383 ermittelt werden soll. Anschließend folgt eine Dosiserweiterungsphase, in der die Dosis bestätigt werden soll.. Ungefähr 270 erwachsene Teilnehmer mit rezidiviertem/refraktärem MM werden an etwa 45 Standorten weltweit in die Studie aufgenommen. Die Teilnehmer erhalten ABBV-383 intravenös (i.v.) in Kombination mit oral/i.v. verabreichtem Pd, oral/i.v. verabreichtem Rd, oral/i.v./subkutan (s.c.) verabreichtem Dd oder oral/i.v. verabreichtem Niro in 21-tägigen Zyklen.
Für die Teilnehmer an dieser Studie kann die Belastung durch die Behandlung höher sein als bei ihrer Standardbehandlung. Während der Studie werden die Teilnehmer regelmäßig untersucht und die Wirkung und etwaige Nebenwirkungen der Behandlung werden häufig durch medizinische Beurteilungen und Blutuntersuchungen und Fragebögen überprüft.
Hintergrund:
ABBV-383 ist ein Prüfpräparat, das für die Behandlung des rezidivierenden/refraktären Multiplen Myeloms entwickelt wird. Es ist ein Antikörper, der (wie Elranatamab und Teclistamab) gegen zwei Ziele gerichtet (bispezifisch) ist: gegen BCMA und gegen CD3. BCMA ist ein Zelloberflächenprotein, das besonders auf Myelom- und Plasmazellen vorkommt und eine besondere biologische Bedeutung für das Überleben der Plasmazelle hat. Es wird bei Menschen mit Multiplem Myelom in signifikant höherem Maße exprimiert. CD3 ist an der Aktivierung der Immunantwort zur Bekämpfung von Infektionen beteiligt.
.
Ein- und Ausschlusskriterien (Auswahl):
Einschlusskriterien:
- Dokumentierte Diagnose eines Multiplen Myeloms gemäß den IMWG-Diagnosekriterien
- ECOG (Index zur Abstufung der Lebensqualität von Patienten mit Krebserkrankungen) von 0, 1 oder2
- Es muss eine bestätigte Diagnose eines rezidivierten/refraktären Multiplen Myeloms (MM) mit dokumentierten Hinweisen auf ein Fortschreiten der Erkrankung während oder nach der letzten Behandlung des Teilnehmers vorliegen, wie vom Prüfarzt anhand der Kriterien der International Myeloma Working Group (IMWG) ermittelt wurde.
- Es muss eine messbare Erkrankung vorliegen, wie im Prüfplan dargelegt.
- Teilnehmer sind bislang nicht mit ABBV-383 vorbehandelt und haben noch nie eine BCMA-gerichtete Therapie erhalten. Teilnehmer, die eine zielgerichtete Therapie gegen Nicht-BCMA-Targets erhalten haben, werden nicht ausgeschlossen.
Ausschlusskriterien:
- Periphere autologe Stammzelltransplantation (SZT) innerhalb von 12 Wochen oder allogene SZT innerhalb eines Jahres vor der ersten Gabe des Studienmedikaments.
- Fortbestehende unerwünschte Ereignisse ≥ Grad 2 (National Cancer Institute [NCI] Common Terminology Criteria for Adverse Events [CTCAE] Version 5.0) infolge einer früheren Krebstherapie.
- Bekannter Myelombefall des zentralen Nervensystems.
Alle weiteren Kriterien besprechen Sie bitte mit Ihrem behandelnden Arzt
Rosenheim
Praxis Pihusch Medizinisches Versorgungszentrum GbR
08031-34511
Traunstein
Klinikum Traunstein
Dr. med. Thomas W Kubin, 0861-705-1243
thomas.kubin@klinikum-traunstein.de
Weiden
Dr. med. Marcus Grüner, Arzt für Innere Medizin Hämatologie und Internistische Onkologie
Würzburg
Medizinische Klinik und Poliklinik II des Universitätsklinikums Würzburg, Zentrum Innere Medizin (ZIM)
0931 201-0 (allgemein)
Studien
AlloRelapseMM
Allogene Stammzelltransplantation im Vergleich zur konventionellen Therapie als Salvage-Therapie für Patienten mit rezidiviertem / progredientem Multiplen Myelom nach einer Erstlinientherapie (AlloRelapseMMStudy)
Organisatorische Daten:
| Prüfplancode: | |
| ISRCTN: | |
| EudraCT: | 2021-001--5-67 |
| Clinicaltrials.gov: | NCT0567319 |
| DRKS: | |
| Sponsor: | Universitätsklinikum Hamburg-Eppendorf mit Unterstützung des Gemeinsamen Bundesausschusses (G-BA) |
| Studienphase: | III |
| Status: | Rekrutierung läuft, geplant bis 6/2027 |
Ziel:
In dieser Studie wird untersucht, ob die Transplantation von gespendeten Stammzellen (allogene Stammzelltransplantation) Vorteile gegenüber der gängigen Therapie bei Patienten mit Multiplem Myelom bietet, bei denen es nach einer Transplantation von körpereigenen Stammzellen (autologe Stammzelltransplantation) als Erstlinientherapie zu einem Erkrankungsrückfall (Rezidiv) oder einem Fortschreiten der Krankheit (Progression) gekommen ist. Es wird geprüft, ob die allogene Stammzelltransplantation das Gesamtüberleben bei diesen Patienten verlängert.
Hintergrund:
Eine Behandlungsoption des Multiplen Myeloms ist die Stammzelltransplantation. Nach einer Chemotherapie, bei der die Krebszellen zerstört werden, werden körpereigene (autologe) oder gespendete körperfremde (allogene) Stammzellen übertragen. Die übertragenen Stammzellen siedeln sich dann im Knochenmark an und bilden „frische“ Blutzellen. Die Stammzelltransplantation kommt als Behandlungsoption nach der ersten Diagnose (Erstlinientherapie), aber auch bei einem Rückfall nach Vorbehandlung (jenseits der Erstlinientherapie) in Frage. Auch wenn das Multiple Myelom oft nicht endgültig heilbar ist, soll die Therapie die Lebenserwartung verlängern und die Symptome zurückdrängen. (Quelle: https://www.g-ba.de/studien/erprobung/allorelapsemmstudy-studie/)
Ein- und Ausschlusskriterien (Auswahl):
Einschlusskriterien:
- Diagnose Multiples Myelom,
- Rückfall (Rezidiv) oder Fortschreiten (Progress) des Multiplen Myeloms unter oder nach einer autologen Stammzelltransplantation
- Erhalt von höchstens 1 Zyklus einer sogenannten Salvage-Therapie (Rezidiv-Therapie) vor Einschluss in die Studie
Ausschlusskriterien:
- Unzureichende Organfunktion gemäß der Definition im Prüfplan
- Aktive Hepatitis B oder C oder unkontrollierte HIV-Infektion
- Andere aktive bösartige Erkrankung
- Vorherige Behandlung mit allogenen Stammzellen
Alle weiteren Kriterien besprechen Sie bitte mit Ihrem behandelnden Arzt.
Doppelblindstudie zur Bewertung der Wirksamkeit und Sicherheit von CAEL-101 bei Patienten mit AL-Amyloidose Stadium IIIa
Organisatorische Daten:
| Prüfplancode: | Cael-101-302 |
| ISRCTN: | |
| EudraCT: | 2020-000713-32 |
| Clinicaltrials.gov: | NCT04512235 |
| DRKS: | |
| Sponsor: | Caelum Biosciences, IQVIA Biotech |
| Studienphase: | 3 |
| Status: | Rekrutierung läuft, geplant bis 08/2022 |
Ziel:
Das Hauptziel dieser Studie ist es, zu ermitteln, ob CAEL-101 mit der Standardtherapie der Plasmazelldyskrasie das Gesamtüberleben bei nicht vorbehandelten Patienten mit AL-Amyloidose im Mayo-Stadium IIIa gegenüber der Standardtherapie für PCD allein verbessern kann.
Hintergrund:
Die AL- (oder Leichtketten-)Amyloidose entsteht im Knochenmark, wo fehlgefaltete Proteine freie Leichtketten bilden. Diese binden aneinander und bilden sogenannte Amyloid-Fibrille, die sich im Raum zwischen den Zellen (dem sogenannten Extrazellularraum) ablagern und zu einer Fehlfunktion des betroffenen Organs führen. (Quelle: https://www.seattlecca.org/trial/nct04512235-a-study-to-evaluate-the-effectiveness-and-safety-of-cael101-in-patients-with-mayo )
CAEL-101 ist ein neuer Anti-Amyloid-Antikörper, der derzeit in der klinischen Phase 3 für die Behandlung von Patienten mit Leichtketten-Amyloidose (AL) geprüft wird.
CAEL-101 hat den Orphan-Drug-Status für seltene Leiden von der amerikanischen Zulassungsbehörde FDA und der Europäischen Arzneimittel-Agentur EMA als Therapie für AL-Amylosidose erhalten. (Quelle: https://caelumbio.com/cael-101/)
Kurzeschreibung:
Dies ist eine doppelblinde, randomisierte, multizentrische internationale Phase-3-Studie mit CAEL-101 in Kombination mit der Standardtherapie für Plasmazelldyskrasie (PCD) im Vergleich zu Placebo in Kombination mit der Standardtherapie für PCD bei Patienten mit AL-Amyloidose im Stadium IIIa nach Mayo, die keine vorherige Behandlung erhalten haben. Die geplante Mindestbehandlungsdauer für jeden Patienten wird mindestens 50 Wochen oder bis zum Tod des Patienten betragen. Es ist geplant, dass alle Patienten die doppelblinde Behandlung so lange fortsetzen, bis der letzte Patient die mindestens 50-wöchige Behandlung abgeschlossen hat.
Ein- und Ausschlusskriterien (Auswahl):
Einschlusskriterien:
- AL-Amyloidose im Mayo-Stadium IIIa bei Patienten mit fortgeschrittener Beteiligung des Herzens zum Zeitpunkt des Screenings
- Messbare hämatologische Erkrankung zum Zeitpunkt des Screenings, definiert durch mindestens einen der folgenden Punkte:
- Differenz zwischen beteiligten und unbeteiligten freien Leichtketten (dFLC) > 4 mg/dl oder
- Beteiligte freie Leichtketten (iFLC) > 4 mg/dl mit abnormem Verhältnis oder
- Serum-Protein-Elektrophorese (SPEP) m-Spike > 0,5 g/d
- Histopathologische Diagnose einer Amyloidose UND Bestätigung von AL-abgeleiteten Amyloid-Ablagerungen durch mindestens eine der folgenden Möglichkeiten:
- Immunhistochemie oder
- Massenspektrometrie oder
- Charakteristisches elektronenmikroskopisches Erscheinungsbild
Ausschlusskriterien:
- Vorliegen einer anderen Form von Amyloidose als einer Amyloidose vom Leichtkettenty (AL)
- Vortherapie für AL-Amyloidose oder multiples Myelom. Die Verabreichung von höchstens 160 mg Dexamethason (oder einem gleichwertigen Kortikosteroid) seit der Diagnose der AL-Amyloidose bis zur Randomisierung ist erlaubt.
- Vorliegen eines multiplen Myeloms oder POEMS-Syndroms nach der Definition der International Myeloma Working Group (IMWG)
Alle weiteren Kriterien besprechen Sie bitte mit Ihrem behandelnden Arzt.
Eine klinische Studie der Phase I/IIa zur Beurteilung der Durchführbarkeit, Sicherheit und Antitumoraktivität von autologen SLAMF7 CAR-T-Zellen beim Multiplen Myelom
Organisatorische Daten:
| Prüfplancode: | Caramba 1 | |
| ISRCTN: | ||
| EudraCT: | 2019-001-264-30 | |
| Clinicaltrials.gov: | NCT04499339 | |
| DRKS: | ||
| Sponsor: |
|
|
| Studienphase: | Phase 1/2a | |
| Status: | Rekrutierung läuft, geplant bis März 2024 |
Ziel:
CARAMBA-1 ist die erste klinische Studie, in der die Anwendung sogenannter SLAMF7Zellen -(engl.: Signaling Lymphocyte Activation Molecule Family Member 7) des chimären Antigenrezeptors (CAR)-T am Menschen untersucht wird. In dieser Studie werden die genetisch veränderten T-Zellen bei Patienten mit fortgeschrittener MM angewendet, bei denen konventionelle Therapien ausgeschöpft sind.
Hintergrund:
Das Multiple Myelom (MM) ist eine seltene hämatologische Malignität von aberranten Plasmazellen.
Es besteht ein hoher und derzeit ungedeckter medizinischer Bedarf an neuartigen, innovativen Behandlungskonzepten zur Verbesserung des therapeutischen Ergebnisses und der Prognose von Patienten, die an MM leiden.
Es gibt definitive Hinweise darauf, dass MM anfällig für immunbasierte Therapien ist, die aus präklinischen Untersuchungen und frühen klinischen Studien stammen.
Die klinische Studie CARAMBA-1 ist eine offene, nicht-randomisierte, multizentrische klinische Studie, die einen Phase I-Dosis-Eskalationsteil mit einem Phase IIa-Dosis-Expansionsteil kombiniert.
In der Phase I werden die Sicherheit der Behandlung mit SLAMF7 CAR-T untersucht und die maximal verträgliche Dosis sowie die für die Phase II empfohlene SLAMF7 CAR-T-Dosis bestimmt.
In der Phase IIa werden die Sicherheit der Behandlung mit SLAMF7 CAR-T untersucht und die Wirksamkeit, definiert als Gesamtansprechrate, von SLAMF7 CAR-T bei Patienten mit MM untersucht. In diesem Teil der Studie werden 25 Patienten mit der SLAMF7 CAR-T behandelt. Nach der CAR-T-Zell-Infusion werden alle Patienten mindestens eine Woche lang Im Krankenhaus überwacht und danach regelmäßig ambulant kontrolliert.
Die Behandlung läuft so ab:
- Die weißen Blutzellen werden mittels Leukapherese extrahiert
- Dann werden die weißen Blutzellen getrennt, um geeignete T-Zellen (Immunzellen) für die genetische Veränderung identifiziert
- “CAR”-Genesequenzen werden in die DNA der T-Zellen eingeführt, um „CAR-T-Zellen“ zu schaffen. Dadurch werden sie in die Lage versetzt, SLAMF7-Protein auf Myelomzellen zu finden und anzugreifen.
- Die veränderten T-Zellen werden dann außerhalb des Körpers expandiert.
- Anschließend werden die T-Zellen wieder in den Körper der Patienten infundiert, wo sie sich vermehren können, wenn ihnen die Zielproteine begegnen, und die Krebszellen abtöten können.
Das CARAMBA-Projekt und die klinische Studie CARAMBA-1 werden von der Europäischen Union im Rahmen des Forschungs- und Innovationsprogramms Horizon 2020 unterstützt.
Weitere Informationen (auf Englisch) unter https://www.caramba-cart.eu/
Ein- und Ausschlusskriterien (Auswahl):
Einschlusskriterien:
- Patient mit der Diagnose MM, der bereits mindestens 2 Behandlungslinien erhalten hat, darunter mindestens ein Zyklus einer Hochdosis-Chemotherapie mit autologer hämatopoetischer Stammzelltransplantation, falls der Patient dafür in Frage kam, und ein immunmodulatorisches Imid-Medikament (z.B. Lenalidomid und/oder Pomalidomid), ein Proteasom-Inhibitor und/oder ein Anti-CD38-Antikörper. (Hinweis: Induktionstherapie, bis zu 2 Zyklen einer Hochdosis-Chemotherapie mit autologer hämatopoetischer Stammzelltransplantation und anschließende Konsolidierungs- und/oder Erhaltungstherapie gelten als eine Behandlungslinie).
- Karnofsky-Leistungsstatus ≥60%. Wenn der Patient einen Karnofsky-Leistungsstatus <60% hat (z.B. nach einer Rückenmarkverletzung), aber vom Untersucher als medizinisch geeignet beurteilt wird, ist der Patient teilnahmeberechtigt.
- Mindestens einer der folgenden Werte müssen gemessen werden:
- Serum M-Protein größer oder gleich 0,5 g/dl
- Urin M-Protein größer oder gleich 200 mg/24 h
- Serumfreier Leichtketten (FLC)-Test: beteiligter FLC-Gehalt größer oder gleich 10 mg/dl (100 mg/l), vorausgesetzt, das Serum-FLC-Verhältnis ist anormal
- Ein durch Biopsie nachgewiesenes auswertbares Plasmozytom
- Anteil der Knochenmark-Plasmazellen in den gesamten Knochenmarkzellen > 10 % (> 30 %, wenn Knochenmark-Plasmazellen der einzige Marker für eine messbare Erkrankung sind)
Ausschlusskriterien:
- Der Patient hat sich in den letzten 12s Monaten vor der Leukapherese einer allogenen Stammzelltransplantation mit entweder Standard- oder reduzierter Konditionierungsintensität unterzogen
- Der Patient hat sich vor mehr als 12 Monaten einer allogenen Stammzelltransplantation mit entweder Standard- oder reduzierter Konditionierungsintensität unterzogen und leidet an chronischer Graft-versus-Host-Disease und/oder erhält systemische Immunsuppressiva
- Der Patient hat in den letzten 8 Wochen vor der Leukapherese Anti-CD38- und/oder Anti-SLAMF7-Antikörper erhalten.
- Der Patient mit Diagnose eines MM
-
- befindet sich in einem ersten Rezidiv nach einer autologen Stammzelltransplantation oder
- in einem zweiten Rezidiv, bei dem anschließend ein komplettes Ansprechen erreicht wird und der Patient dann für eine allogene Stammzelltransplantation infrage kommt, sofern der Patient eine allogene Stammzelltransplantation nicht ausdrücklich ablehnt
Alle weiteren Kriterien besprechen Sie bitte mit Ihrem behandelnden Arzt.
Studie mit Iberdomid
Eine Studie zur Bestimmung der Dosis und Verträglichkeit der CC-220 Monotherapie mit Iberdomid, in Kombination mit Dexamethason und in Kombination mit Dexamethason und Daratumumab oder Bortezomib bei Patienten mit fortgeschrittenem und refraktärem Multiplem Myelom (RRMM)
Organisatorische Daten:
| Prüfplancode: | CC-220-MM-001 |
| ISRCTN: | |
| EudraCT: | 2016-000860-40 |
| Clinicaltrials.gov: | NCT02773030 |
| DRKS: | |
| Sponsor: | Celgene |
| Studienphase: | Phase 1b/2a |
| Status: | Rekrutierung läuft, geplant bis Mai 2026 |
Ziel:
Dies ist eine multizentrische, länderübergreifende, offene Phase-1b/2a-Dosiseskalationsstudie zur Bestimmung der höchsten verträglichen Dosis, der Sicherheit, Verträglichkeit, Pharmakokinetik (Einwirkung des Körpers auf die Substanz)und Wirksamkeit von CC-220 (Iberdomid) als Monotherapie und in Kombination mit anderen Therapien bei Patienten mit rezidivierendem oder therapierefraktärem Multiplem Myelom.
Hintergrund:
Iberdomid (CC-220) ist eine neuartige Substanz, die in dieser Phase I/II Studie zur Behandlung von fortgeschrittenem und refraktärem Multiplem Myelom in Kombination mit anderen Therapien untersucht wird. Präklinische Studien zu Iberdomid zeigen, dass es wirksamer an das Protein Cereblon bindet als andere Cereblon-bindende Substanzen. Klinische Studien zu Bortezomib und Daratumumab in Kombination mit anderen Cereblon-bindenden Mitteln haben eine hohe Verträglichkeit bei bemerkenswerter Wirksamkeit bei RRMM gezeigt. Allerdings wurden diese Kombinationen mit Iberdomid bisher nicht untersucht. Insgesamt gesehen untermauern die vorliegenden präklinischen Daten die Untersuchung von Iberdomid in Kombination mit sowohl Bortezomib/Dexamethason als auch Daratumumab in klinischen Studien.
(Michael Amatangelo et al, Blood 2018. 132, 1935; http://www.bloodjournal.org/content/132/Suppl_1/1935?sso-checked=true
Durchführung:
Die Studie wird in zwei Teilen durchgeführt: Teil 1 mit Kohorte A und B und Teil 2 mit Kohorte C, D, E, F, G1 und G2.
In Teil 1 (Phase 1b) wird die maximal verträgliche Dosis von oralem CC-220 als Monotherapie (Kohorte A) und die von oralem CC-220 in Kombination mit oralem Dexamethason (Kohorte B) bestimmt. Außerdem wird in diesem Teil die empfohlene CC-220-Dosis für Teil 2 (Phase 2) ermittelt.
In Teil 2 werden folgende Therapien untersucht:
Kohorte C: CC-220 als Monotherapie in der empfohlenen Dosis für Teil 2
Kohorte D: CC-220 in der empfohlenen Dosis für Teil 2 in Kombination mit oralem Dexamethason
Kohorte E:CC-220 in Kombination mit oralem Dexamethason und intravenösem Daratumumab
Kohorte F: CC-220 in Kombination mit oralem Dexamethason und subkutanem Bortezomib
Kohorte G1: CC-220 in Kombination mit einmal wöchentlich verabreichtem intravenösem Carfilzomib und oralem Dexamethason
Kohorte G2: CC-220 in Kombination mit zweimal wöchentlich verabreichtem intravenösem Carfilzomib und oralem Dexamethason.
Ein- und Ausschlusskriterien (Auswahl):
Einschlusskriterien:
- Dokumentierte Diagnose eines Multiplen Myeloms (MM) und messbare Krankheit, definiert als
- M-Protein: Serum-Elektrophorese ≥ 0,5 g/dl und/oder Urinprotein-Elektrophorese ≥ 200 mg/24 Stunden und/oder
- Leichtketten-Myelom ohne messbare Erkrankung im Serum oder Urin - Dokumentierte Krankheitsprogression an oder innerhalb von 60 Tagen seit der letzten Dosis der letzten Myelombehandlung
- ECOG (Index zur Abstufung der Lebensqualität von Patienten mit Krebserkrankungen) von 0, 1 oder 2
Ausschlußkriterien:
- Nicht ekretorisches oder oligosekretorisches Multiples Myelom
- Plasmazellenleukämie oder Amyloidose
- Bestimmte Laborwerte, die nicht im Normalbereich liegen
- Periphere Neuropathie ≥ Grad 2
Alle weiteren Kriterien besprechen Sie bitte mit Ihrem behandelnden Arzt.
Ein neuer Cereblon E3 Ligase Modulator
Eine Studie zur Bestimmung der empfohlenen Dosis und des Regimes und zur Bewertung der Sicherheit und vorläufigen Wirksamkeit von CC-92480 in Kombination mit Standardbehandlungen bei Patienten mit rezidiviertem oder refraktärem Multiplen Myelom (RRMM) und neu diagnostiziertem Multiplen Myelom (NDMM)
Organisatorische Daten:
| Prüfplancode: |
CC-92480-mm-02 |
| UTMS | U1111-1233-5619 |
| EudraCT: | 2018-004767-31 |
| Clinicaltrials.gov: | NCT03989414 |
| DRKS: | |
| Sponsor: | Celgene |
| Studienphase: | Phase 1/2 |
| Status: | Rekrutierung läuft, geplant bis Januar 2025 |
Hintergrund:
CC-92480 ist ein sogenannter CRBN-Modulator [Cereblon-(CRBN-)E3-Ligase-Modulator (CELMoD)]. Dieser neuartige Modulator hat vielfältige Wirkungen und wirkt unter anderem stark immunmodulierend. Der Wirkstoff führt zu einem schnellen, tiefen und anhaltenden Zerfall von Ikaros und Aiolos – zwei Faktoren, die zum Überleben der Myelomzellen beitragen.
Durchführung:

Die Studie wird randomisiert ausgeführt und die Patienten in 3 Gruppen eingeteilt, die neben dem CC-92480 unterschiedliche Zweier-Kombinationen enthalten, die gegeneinander getestet werden. Die Kohorten haben unterschiedliche Einschlusskriterien.
Ein und Ausschlusskriterien:
Einschlusskriterien:
- Alter ≥ 18 Jahre alt und ECOG (Index zur Abstufung der Lebensqualität von Patienten mit Krebserkrankungen) mit 0, 1 oder 2 Punkten.
- Patienten mit rezidiviertem oder refraktäremMultiplen Myelom müssen eine messbare Krankheit haben und ihr Krankheitsverlauf während oder nach ihrer letzten Myelomtherapie muss dokumentiert sein.
- Bei neu diagnostizierten Patienten muss die Diagnose eines zuvor unbehandelten symptomatischen Multiplen Myeloms dokumentiert sein.
- Frauen im gebärfähigen Alter und männliche Patienten müssen mit dem Schwangerschaftsverhütungsplan einverstanden sein.
Ausschlusskriterien:
- Signifikante medizinische Erkrankung, auffällige Laborwerte oder eine psychiatrische Krankheit, die an der Teilnahme an der Studie hindert.
- Patient ist nicht in der Lage oder nicht bereit, sich der laut Prüfplan vorgeschriebenen Prophylaxe einer Thromboembolie zu unterziehen.
Alle weiteren Kriterien besprechen Sie bitte mit Ihrem behandelnden Arzt
TCR-Immuntherapie mit MDG1011
Erste Phase-1/2-Studie mit TCR-Immuntherapie MDG1011 am Menschen.
Diese Dosisfindungsstudie bewertet die Sicherheit, Durchführbarkeit und vorläufige Wirksamkeit von genmodifizierten T-Zellen bei Patienten mit myeloischen und lymphatischen Neoplasien, die mit einem hohen Risiko einhergehen.
Im Phase-1-Teil dieser multizentrischen, offenen klinischen Phase-1/2-Studie sollen ca. 12 Patienten behandelt werden, die HLA-A*02:01-positiv sind und an fortgeschrittenen hämatologischen Erkrankungen wie akuter myeloischer Leukämie (AML), myelodysplastischem Syndrom (MDS) oder multiplem Myelom (MM) leiden. Die Expression von PRAME ist eine weitere Voraussetzung zur Teilnahme an dieser Dosis-Eskalations-Studie. PRAME ist ein Krebs-Antigen, welches den Zelltod und die Zelldifferenzierung hemmt und vermutlich an der malignen Entartung beteiligt ist.
In drei Dosiskohorten und einer optionalen vierten Dosiskohorte werden Dosisbereiche von 100.000 bis 10.000.000 transduzierten (gen-modifizierten) T-Zellen pro kg Körpergewicht getestet. Jede Dosiskohorte wird je einen Patienten aus jeder der drei hämatologischen Erkrankungen enthalten. Die Patienten werden eine Vorbehandlung mit Cyclophosphamid und Fludarabin erhalten. Nach der vollständigen Behandlung aller Patienten einer Dosiskohorte und einer vierwöchigen Beobachtungsperiode zur Sicherheit wird ein unabhängiges "Data Safety and Monitoring Board" (DSMB) über den Start der nächsten Dosisgruppe entscheiden.
Organisatorische Daten:
| Prüfplancode: | CD-TCR-001 |
| ISRCTN: | |
| EudraCT: | 2017-000440-18 |
| Clinicaltrials.gov: | NCT03503968 |
| DRKS: | |
| Sponsor: | Medigene AG |
| Studienphase: | 1/2 |
| Status: | Rekrutierung läuft, geplant bis August 2020 |
Ziel:
Die primären Endpunkte für den Phase-1-Teil der klinischen Studie sind Sicherheit und Verträglichkeit von MDG1011, die maximal verträgliche Dosis und die für die Phase 2 empfohlene Dosis sowie die Durchführbarkeit. Als weitere Endpunkte werden die Gesamtansprechrate, die Dauer des Ansprechens, die Zeit bis zur Krankheitsprogression, das progressionsfreie Überleben, das Gesamtüberleben, die Lebensqualität und der Zusammenhang zwischen der PRAME-Expression mit der Antitumor-Antwort nach drei Monaten beurteilt. Insgesamt beträgt die Nachbeobachtungszeit bis zu 12 Monate.
Die Endpunkte des Phase-2-Teils sind die weitere Bewertung der Sicherheit und Wirksamkeit, wobei die Wirksamkeit als Gesamtansprechrate nach 3 Monaten gemessen wird. Die Studie wird eine Nachbeobachtungszeit von bis zu 12 Monaten haben. Weitere Endpunkte umfassen die Dauer des Ansprechens, die Zeit bis zur Progression, das progressionsfreie Überleben, das Gesamtüberleben, die Lebensqualität, die Durchführbarkeit und den Zusammenhang der PRAME-Expression mit der Antitumor-Antwort.
Die experimentelle TCR-Therapie MDG1011 wird im Rahmen dieser Studie erstmals am Menschen geprüft.
Hintergrund:
Die TCR-Technologie zielt darauf ab, körpereigene T-Zellen des Patienten mit tumorspezifischen T-Zell-Rezeptoren auszustatten. Die bezüglich ihres Rezeptors modifizierten T-Zellen sind dadurch in der Lage, Tumorzellen zu erkennen und wirksam zu zerstören. Dieser immuntherapeutische Ansatz versucht, die bestehende Toleranz gegenüber den Krebszellen und die tumor-induzierte Immunsuppression im Patienten zu überwinden, indem T-Zellen des Patienten außerhalb des Körpers aktiviert und modifiziert werden.
Ein- und Ausschlusskriterien (Auswahl):
Einschlusskriterien (allg.):
- Dokumentierte Diagnose der Erkrankung im letzten Stadium in den letzten 4 Wochen vor dem Screening
- Humanes Leukozytenantigen (HLA)
- Phase 1 und Phase 2 (Behandlungsgruppe): Nachweis von HLA-A*02:01
- Phase 2 (Vergleichsgruppe): kein Nachweis von HLA-A*02:01
- Lebenserwartung von mindestens 4 Monaten
- ECOG (Index zur Abstufung der Lebensqualität von Patienten mit Krebserkrankungen) von 0 bis 2
- keine geplante allogene hämatopoetische Stammzelltransplantation (HSZT)
Multiples Myelom-(MM-)spezifische Einschlusskriterien:
- Rezidiviertes und refraktäres MM
- Mindestens 3 vorangegangene Therapielinien mit mindestens einem Proteasomeninhibitor und einer immunmodulierenden Substanz (IMiD). Eine Induktion mit oder ohne hämatopoetische Stammzelltransplantation und mit oder ohne Erhaltungstherapie wird als ein einziges Behandlungsschema betrachtet.
- Myelomzellen müssen PRAME positiv exprimieren
Ausschlußkriterien:
- Akute Promyelozyten-Leukämiamit t(15;17)(q22;q12); Promyelozyten-Leukämia/Retinoic Acid Receptor Alpha (PML-RARA) oder mit varianten Translokationen
- Bekannter Nachweis des HIV-Virus, aktive Hepatitis-B-Virus-(HBV-) oder Hepatitis-C-Virus-(HCV-)Infektion
- Klinisch signifikante, fortgeschrittene oder instabile Erkrankung oder unzureichende Funktion eines Hauptorgans, die den Teilnehmer einem besonderen Risiko aussetzen könnte
- allogene Stammzelltransplantation in der Vorgeschichte
MM-spezifische Ausschlusskriterien für Phase 1 und Phase 2 (Behandlungsgruppe, falls das MM in Phase 2 fortschreitet):
- Vortherapie mit immunmodulierenden Substanzen (IMiDs) innerhalb von 14 Tagen vor der Leukapherese und/oder der Infusion des Prüfpräparats
- Vortherapie mit Kortikosteroiden innerhalb von 7 Tagen vor der Leukapherese oder 7 Tagen vor der Infusion des Prüfpräparats
Alle weiteren Kriterien besprechen Sie bitte mit Ihrem behandelnden Arzt.
Belantamab-Mafodotin
Bewertung der Wirksamkeit und Sicherheit von Belantamab-Mafodotin, Bortezomib und Dexamethason gegenüber Daratumumab, Bortezomib und Dexamethason bei Teilnehmern mit rezidiviertem/refraktärem Multiplen Myelom
Organisatorische Daten:
| Prüfplancode: | 207503 |
| ISRCTN: | |
| EudraCT: | 2018-003993-29 |
| Clinicaltrials.gov: | NCT04246047 |
| DRKS: | |
| Sponsor: | GlaxoSmithKline |
| Studienphase: | III |
| Status: | Rekrutierung geplant bis Juni/2026 |
Kurzbeschreibung:
Hierbei handelt es sich um eine randomisierte, offene Phase-3-Studie zur Untersuchung der Sicherheit und Wirksamkeit von Belantamab-Mafodotin in Kombination mit Bortezomib/Dexamethason (Arm A) gegenüber Daratumumab in Kombination mit Bortezomib/Dexamethason (Arm B) bei Teilnehmern mit rezidivierendem multiplem Myelom..
Hintergrund:
Die amerikanische Arzneimittelbehörde FDA hat Belantamab-Mafodotin-blmf (GSK2857916; Blenrep) für die Behandlung von Patienten mit rezidiviertem oder refraktärem Multiplen Myelom zugelassen, die zuvor mit mindestens 4 Therapien behandelt wurden, darunter ein immunmodulatorisches Mittel, ein Proteasom-Inhibitor und ein Anti-CD38-Antikörper. Dies ist weltweit die erste Anti-BCMA-Behandlung, die bei dieser Patientenpopulation verfügbar ist.
Belantamab-Mafodotin ist gegen das B-Zell-Reifungsantigen (BCMA) gerichtet, das eine wichtige Rolle für das Überleben von Plasmazellen spielt und auf Zellen des Multiplen Myeloms exprimiert wird. Das Antikörper-Wirkstoff-Konjugat Belantamab-Mafodotin bindet an BCMA auf Myelom-Zelloberflächen, wodurch der Zellzyklus angehalten und eine antikörperabhängige zelluläre Zytotoxizität induziert wird.
Normalerweise fördert BCMA das Überleben von Plasmazellen durch Signalübertragung von zwei bekannten Liganden. Dieser Signalweg hat sich als wichtig für das Wachstum und Überleben von Myelomzellen erwiesen.
Ein- und Ausschlusskriterien (Auswahl):
Einschlusskriterien:
- Bestätigte Diagnose eines Multiplen Myeloms (MM) gemäß IMWG-Kriterien
- Vorbehandlung des MM mit mindestens einer Therapielinie und dokumentierte Krankheitsprogression während oder nach der letzten Therapie.
- ECOG Performance Status (Index zur Abstufung der Lebensqualität von Patienten mit Krebserkrankungen) von 0 bis 2
- Muss mindestens 1 Aspekt einer messbaren Erkrankung aufweisen, wie folgt definiert:
- Urin-M-Protein-Ausscheidung > 200 mg pro 24 Stunden, oder
- Serum-M-Protein-Konzentration > 0,5 g/dl, oder
- Freie Leichtketten im Serum (FLC): beteiligter FLC-Spiegel > 10 mg/dl (> 100 mg/L) und ein abnormes Verhältnis der freien Leichtketten im Serum (< 0,26 oder > 1,65).
- Alle Nebenwirkungen, die infolge durch Vorbehandlungen hervorgerufen wurden, müssen zum Zeitpunkt der Rekrutierung < Grad 1 sein, mit Ausnahme von Alopezie.
Ausschlußkriterien:
- Unverträglichkeit gegenüber Daratumumab.
- Kein bzw. kein hinreichendes Ansprechen (therapierefraktär) gegenüber Daratumumab oder einer anderen Anti-CD38-Therapie (definiert als fortschreitende Erkrankung während der Behandlung mit einer Anti-CD38-Therapie oder innerhalb von 60 Tagen nach Abschluss dieser Behandlung).
- Unverträglichkeit gegenüber Bortezomib oder kein bzw. kein hinreichendes Ansprechen (therapierefraktär) gegenüber Bortezomib (definiert als fortschreitende Erkrankung während der Behandlung mit einem Bortezomib-haltigen Schema von 1,3 mg/m2 zweimal wöchentlich oder innerhalb von 60 Tagen nach Abschluss dieser Behandlung). Hinweis: Patienten mit fortschreitender Erkrankung während der Behandlung mit einem wöchentlichen Bortezomib-Schema dürfen teilnehmen.
- Anhaltende periphere Neuropathie von Grad 2 oder höher oder neuropathische Schmerzen.
- Vorherige Behandlung mit einer Anti-B-Zellreifungsantigen- (Anti-BCMA-) Therapie.
Alle weiteren Kriterien besprechen Sie bitte mit Ihrem behandelnden Arzt.
Belantamab-Mafodotin
Eine Phase-III-Studie zu Belantamab-Mafodotin plus Pomalidomid und Dexamethason vs.Pomalidomid, Bortezomib und Dexamethason bei Studienteilnehmern mit rezidiviertem/refraktärem
multiplem Myelom (RRMM)
Organisatorische Daten:
| Prüfplancode: | 207499 |
| ISRCTN: | |
| EudraCT: | 2018-004354-21 |
| Clinicaltrials.gov: | NCT04484623 |
| DRKS: | |
| Sponsor: | GlaxoSmithKline |
| Studienphase: | III |
| Status: | Rekrutierung geplant bis Jani/2027 |
Ziel:
Der primäre Endpunkt der Studie ist das progressionsfreie Überleben. Sekundäre Endpunkte sind u.a. die Erfassung des Überlebens, der Ansprechrate, der Dauer des Ansprechens sowie Aspekte zur Sicherheit und Lebensqualität.
Hintergrund:
Bei der Studie DREAMM-8 handelt es sich um eine offene, randomisierte Phase-III-Studie zur Beurteilung der Wirksamkeit und der Sicherheit von Belantamab-Mafodotin in Kombination mit
Pomalidomid und Dexamethason (B-Pd) im Vergleich zu Pomalidomid, Bortezomib und Dexamethason (PVd) bei Studienteilnehmern mit RRMM, die mit Lenalidomid vorbehandelt wurden
und mindestens 1 vorherige Therapielinie erhalten haben.
Die Studienteilnehmer werden in einem Verhältnis von 1:1 zentral in einen der beiden Behandlungsarme randomisiert. Es ist geplant ca. 450 Patienten in die Studie aufzunehmen. Diese
werden bis zum Eintreten eines der folgenden Ereignisse behandelt: Fortschreiten der Erkrankung, Tod, schwere Nebenwirkungen, Beginn einer neuen Krebsbehandlung, Ausscheiden aus eigenem Wunsch oder Studienende.
Ein- und Ausschlusskriterien (Auswahl):
Einschlusskriterien:
- Der Patient muss eine bestätigte Diagnose des Multiplen Myeloms gemäß den IMWG-Kriterien
haben - Performance-Status der Eastern Cooperative Oncology Group (ECOG - Index zur Abstufung der
Lebensqualität von Patienten mit Krebserkrankungen) von 0 bis 2 - Der Teilnehmer muss zuvor mit mindestens einer vorherigen MM-Therapielinie einschließlich
eines Lenalidomid enthaltenden Behandlungsschemas behandelt worden sein und das
Fortschreiten der Krankheit muss während oder nach seiner letzten Therapie dokumentiert
worden sein - Der Teilnehmer hat sich einer autologen Stammzellentransplantation unterzogen oder gilt als
nicht transplantationsfähig - Adäquate Organsystem-Funktionen, die im Protokoll genau definiert sind
Ausschlußkriterien:
- Aktive Plasmazell-Leukämie zum Zeitpunkt des Screenings. Symptomatische Amyloidose, aktives
POEMS-Syndrom (Polyneuropathie, Organomegalie, Endokrinopathie, monoklonale
Plasmaproliferationsstörung und Hautveränderungen) - Systemische Anti-Myelom-Therapie (einschließlich Chemotherapie und systemischer Steroide)
oder Verwendung eines Prüfpräparats innerhalb von 14 Tagen oder fünf Halbwertszeiten vor
der ersten Dosis des Prüfmedikaments - Vorherige Behandlung mit einem monoklonalen Antikörpermedikament innerhalb von 30 Tagenvor Erhalt der ersten Dosis der Prüfmedikamente.
- Vorherige gezielte BCMA-Therapie
Alle weiteren Kriterien besprechen Sie bitte mit Ihrem behandelnden Arzt.
Teclistamab, Daratumumab, Lenalidomid,Dexamethason +/- Bortezomib
Phase-2-Studie zur Bewertung der Sicherheit und Wirksamkeit von Teclistamab in Kombination mit Daratumumab, Lenalidomid und Dexamethason mit und ohne Bortezomib als Induktionstherapie und Teclistamab in Kombination mit Daratumumab und Lenalidomid als Erhaltungstherapie bei transplantationsgeeigneten Patienten mit neu diagnostiziertem Multiplem Myelom
Organisatorische Daten:
| Prüfplancode: | GMMG-HD10, DSMM-XX, 64007957MMY2003, MajesTEC-5 |
| ISRCTN: | |
| EudraCT: | |
| Clinicaltrials.gov: | NCT05695508 |
| DRKS: | |
| Sponsor: | Universitätsklinikum Heidelberg in Zusammenarbeit mit Janssen |
| Studienphase: | Phase 3 |
| Status: | Rekrutierung läuft, geplant bis Mai 2026 |
Hintergrund:
Teclistamab ist ein bispezifischer Antikörper, der an das B-Zell-Reifungsantigen (BCMA), ein Protein auf der Oberfläche von Myelomzellen, bindet und gegen CD3-Rezeptoren auf der Oberfläche von T-Zellen gerichtet ist. Teclistamab wurde im August 2022 in der EU als Monotherapie zur Behandlung des fortgeschrittenen Multiplen Myeloms zugelassen und wird jetzt bei weiteren Indikationen geprüft.
In dieser Studie bei Patienten mit neu diagnostiziertem Multiplem Myelom, die für eine Transplantation geeignet sind, werden die Sicherheit, Verträglichkeit und Wirksamkeit einer Fünffach-Kombination in der Induktionstherapie geprüft: Teclistamab (Tec) in Kombination mit Daratumumab (Dara), Lenalidomid (R), Bortezomib (V) und Dexamethason (d).
Durchführung
Das Studiendesign gliedert sich in drei Studienarme:
Patienten in Arm A und B erhalten eine Induktionstherapie mit Tec-Dara-Rd (Arm A) oder Tec-Dara-VRd (Arm B). Es folgen eine Hochdosis-Chemotherapie und eine autologe Stammzelltransplantation gemäß Therapiestandard sowie eine Erhaltungstherapie mit Tec-Dara-R.
Patienten in Arm C erhalten eine Induktionstherapie gemäß Therapiestandard gefolgt von einer Hochdosis-Chemotherapie und einer autologen Stammzelltransplantation sowie gegebenenfalls einer Konsolidierungstherapie. Im Anschluss daran folgt eine Erhaltungstherapie mit Tec-Dara-R.
Die Behandlungsdauer der Induktionsphase beträgt 6 Zyklen (à 28 Tage). Im Anschluss daran folgen eine Hochdosis-Chemotherapie und autologe Stammzelltransplantation . Danach beginnt die Erhaltungsphase der Studie unter Tec-Dara-R über 18 Zyklen.
Studienarm C beginnt mit dem Screening nach abgeschlossener Hochdosis-Chemotherapieplus autologer Stammzelltransplantation. Die Behandlung erfolgt genauso wie in Arm A und B mit Tec-Dara-R als Erhaltungstherapie für 18 Zyklen.
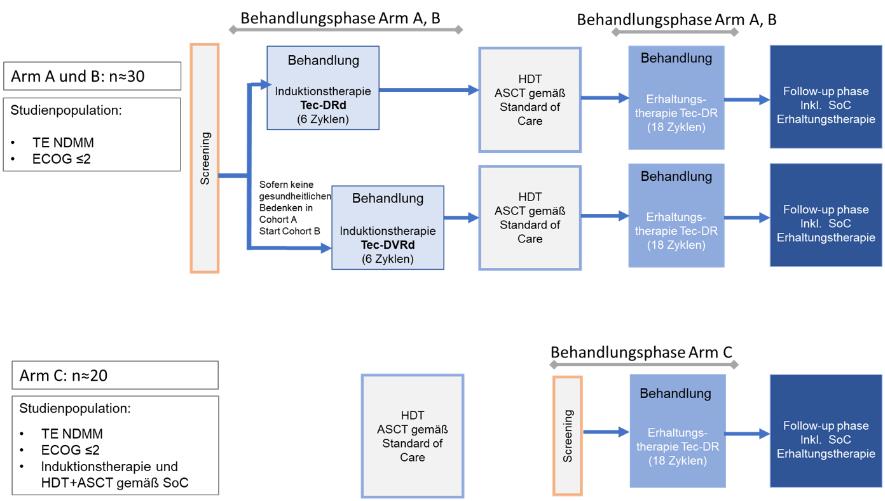
Abb. Studiendesign, mit freundlicher Genehmigung des Universitätsklinikums Heidelberg, Prof. Raab
Ein- und Ausschlusskriterien (Auswahl):
Einschlusskriterien:
- Neu diagnostiziertes Multiples Myelom gemäß den Diagnosekriterien der International Myeloma Working Group (IMWG) und Erhalt einer Induktionstherapie mit oder ohne Konsolidierung
- Ein ECOG-Performance-Status-Score (Index zur Abstufung der Lebensqualität von Patienten mit Krebserkrankungen) von 0, 1 oder 2 beim Screening und unmittelbar vor Beginn der Verabreichung der Studienbehandlung
- Messbare Erkrankung während der Screening-Phase, gemäß der Definition im Protokoll
Ausschlußkriterien
- Beteiligung des ZNS oder klinische Anzeichen für eine Beteiligung der Hirnhäute
- Schlaganfall oder Krampfanfall innerhalb von 6 Monaten vor Studienbeginn
- Transplantation in der Krankengeschichte, die eine immunsuppressive Behandlung erforderte
Alle weiteren Kriterien besprechen Sie bitte mit Ihrem behandelnden Arzt.
Induktionstherapie mit Lenalidomid, Bortezomib und Dexamethason und entweder intravenösem oder subkutanem Isatuximab bei Patienten mit neu diagnostiziertem Multiplem Myelom, die für eine Hochdosis-Chemotherapie mit nachfolgender autologer Stammzelltransplantation geeignet sind
Organisatorische Daten:
| Prüfplancode: | GMMG-HD 8 / DSMM XIX |
| ISRCTN: | |
| EudraCT: | 2022-000996-38 |
| Clinicaltrials.gov: | NCT05804032 |
| DRKS: | |
| Sponsor: | Universitätsklinikum Heidelberg DSMM, Sanofi und KKS-Netzwerk |
| Studienphase: | |
| Status: | Rekrutierung geplant bis Juni 2025 |
Ziel:
In dieser Studie für Patienten mit zuvor unbehandeltem Multiplem Myelom soll die Wirksamkeit der Induktionstherapie mit Isatuximab in Kombination mit Lenalidomid/Bortezomib/Dexamethason (RVd) bei Gabe von Isatuximab unter die Haut (subkutan) gegenüber einer Gabe in die Vene (intravenös) untersucht werden.
Durchführung:
Randomisierung: Die Patienten werden vor der Induktionstherapie nach dem Zufallsverfahren (randomisiert) einem von 2 Studienarmen (A oder B) zugeordnet.
- Patienten in Arm A erhalten 3 Zyklen des monoklonalen Antikörpers Isatuximab intravenös in Kombination mit dem RVd-Schema (Lenalidomid, Bortezomib, Dexamethason). Jeder Zyklus hat eine Dauer von 42 Tagen.
- Patienten in Arm B erhalten 3 Zyklen Isatuximab subkutan in Kombination mit RVd.
Nach der Induktionstherapie erhalten die Patienten eine Standard-Intensivierung (in der Regel eine Mobilisierungstherapie auf Cyclophosphamid-Basis, Stammzellenentnahme und hochdosiertes Melphalan, gefolgt von einer autologen Stammzelltransplantation
Ein- und Ausschlusskriterien (Auswahl):
Einschlusskriterien:
- Bestätigte Diagnose eines neu diagnostizierten behandlungsbedürftigen Multiplen Myeloms gemäß den überarbeiteten Diagnosekriterien der International Myeloma Working Group (IMWG))
- Der Patient ist für eine Hochdosis-Chemotherapie und eine autologe Stammzelltransplantation geeignet
- Messbare Krankheitsaktivität (gemäß der Definition im Prüfplan)
- Alter 18 bis 70 Jahre bei Studieneinschluss
Ausschlußkriterien:
- Bekannte Überempfindlichkeit (oder Kontraindikation) gegen einen der Bestandteile der Studientherapie
- Systemische Amyloid-Leichtketten-Amyloidose (außer lokalisierte Amyloid-Leichtketten -Amyloidose, die auf die Haut oder das Knochenmark beschränkt ist)
- Plasmazell-Leukämie
- Vorherige Chemo- oder Strahlentherapie in den letzten 5 Jahren (außer lokaler Strahlentherapie bei lokalem Fortschreiten des Myeloms)
Alle weiteren Kriterien besprechen Sie bitte mit Ihrem behandelnden Arzt.
CAR T-Zelltherapie mit bb2121
Eine Phase-2-Studie zur Bestimmung der Wirksamkeit und Sicherheit von bb2121 bei Patienten mit rezidiviertem (wieder aufgetretenem) und refraktärem (nicht auf Behandlung ansprechendem) Multiplem Myelom (RRMM) und bei Patienten mit risikoreichem Multiplem Myelom, bei denen die Krankheit innerhalb von 18 Monaten nach der Erstbehandlung fortgeschritten ist.
Organisatorische Daten:
| Prüfplancode: | KarMMa2 |
| ISRCTN: | |
| EudraCT: | 2018-000264-28 |
| Clinicaltrials.gov: | NCT03601078 |
| DRKS: | |
| Sponsor: | Celgene |
| Studienphase: | Phase 2 |
| Status: | Rekrutierung läuft, geplant bis März 2025 |
Ziel:
In dieser Studie soll die Wirksamkeit und Sicherheit von bb2121 bei Patienten mit rezidiviertem oder refraktären Multiplen Myelom bewertet werden.
Hintergrund:
Die chimäre-Antigenrezeptor-(CAR) T-Zelltherapie bb2121 ist gegen das Oberflächenantigen BCMA (engl. B-cell maturation antigen) gerichtet, um T-Zellen dahin gehend zu programmieren, dass sie maligne Myelomzellen erkennen und abtöten. https://meetinglibrary.asco.org/record/160693/abstract
In einer Phase-1-Studie bei stark vorbehandelten Patienten mit rezidiviertem oder refraktären multiplem Myelom zeigte bb2121 ermutigende Ergebnisse mit tiefem und dauerhaftem Ansprechen bei gleichzeitig guter Verträglichkeit. https://www.presseportal.de/pm/62626/3972298 In der vorliegenden Studie soll die Wirksamkeit und Sicherheit von bb2121 als mögliche Therapie für Multiples Myelom weiter untersucht werden.
Ein- und Ausschlusskriterien (Auswahl):
Einschlusskriterien:
- Es besteht eine messbare Krankheit, definiert als
- M-Protein (Serum-Protein-Elektrophorese [sPEP] oder Urin-Protein-Elektrophorese [uPEP]): sPEP ≥ 0,5 g/dl oder uPEP ≥ 200 mg/24 Stunden und/oder
- Leichtketten-MM ohne messbare Krankheit im Serum oder Urin: freie Leichtketten im Serum ≥ 10 mg/dl und abnormes Kappa-Lambda-Leichtketten-Verhältnis im Serum
- Spezifische Anforderungen für:
- Kohorte 1: ≥ 3 frühere Anti-Myelom-Behandlungsschemen
- Kohorte 2: 1 frühere Anti-Myelom-Behandlung
- ECOG Performance Status von 0 oder 1 ((Index zur Abstufung der Lebensqualität von Patienten mit Krebserkrankungen)
Ausschlusskriterien:
- Erhalt eines Prüfpräparats innerhalb von 14 Tagen vor der Leukapherese
- Eines der folgenden Verfahren innerhalb der letzten 14 Tage vor der Leukapherese:
- Plasmapherese
- Große Operation (nach Definition des Prüfarztes)
- Strahlentherapie mit Ausnahme der lokalen Therapie für myelombedingten Knochenläsionen
- Anwendung einer systemischen Anti-Myelom-Medikamententherapie
- Bekannte Beteiligung des zentralen Nervensystems
- Klinischer Nachweis einer Lungenleukostase und Verbrauchskoagulopathie (disseminierten intravasale Gerinnung)
- Vorgeschichte oder Vorliegen einer klinisch relevanten Erkrankung des Zentralnervensystems (ZNS)
Alle weiteren Kriterien besprechen Sie bitte mit Ihrem behandelnden Arzt.
Ergänzende Informationen
Zur Herstellung der mit einem bb2121 chimären Antigenrezeptor (CAR) modifizierten T-Zellen werden die weißen Blutkörperchen (Leukozyten) aus dem Blut herausgelöst. Dies bezeichnet man als Leukapherese. Vor der bb2121-Infusion wird bei den Patienten ein Verfahren zur Entfernung der Lymphozyten, die sogenannte Lymphozytendepletion, mit Fludarabin und Cyclophosphamid durchgeführt.
Intravenös verabreichtes ABBV-383 in Kombination mit Krebstherapien bei Patienten mit rezidiviertem oder refraktärem Multiplen Myelom: eine Studie zur Bewertung der unerwünschten Ereignisse und der Veränderung der Krankheitsaktivität
Organisatorische Daten:
NCT05259839
| Prüfplancode: |
M22-947 |
| ISRCTN: | |
| EudraCT: | |
| Clinicaltrials.gov: | NCT05259839 |
| DRKS: | |
| Sponsor: | TeneoOne Inc |
| Studienphase: | Phase 1, Erstanwendung am Menschen |
| Status: | Rekrutierung läuft, geplant bis Okt.2028 |
Ziele:
Das Multiple Myelom (MM) ist eine Plasmazellerkrankung, die durch das Wachstum klonaler Plasmazellen im Knochenmark gekennzeichnet ist. Ziel dieser Studie ist es, die Sicherheit und Toxizität von ABBV-383 bei gleichzeitiger Verabreichung mit Pomalidomid-Dexamethason (Pd), Lenalidomid-Dexamethason (Rd), Daratumumab-Dexamethason (Dd) oder Nirogacestat (Niro) bei erwachsenen Teilnehmern mit rezidiviertem/refraktärem Multiplem Myelom (MM) zu untersuchen. Es werden unerwünschte Ereignisse und Veränderungen der Krankheitsaktivität bewertet.
Durchführung:
In dieser Studie werden die Teilnehmer in Gruppen eingeteilt, die als Behandlungsarme bezeichnet werden. Untersucht wird ABBV-383 in Kombination mit Pd, Rd, Dd oder Niro. Jeder Behandlungsarm erhält eine andere Behandlungskombination, je nach Stadium der Studie und Eignung des Teilnehmers. Die Studie umfasst eine Dosissteigerungsphase, in der die beste Dosis von ABB-383 ermittelt werden soll. Anschließend folgt eine Dosiserweiterungsphase, in der die Dosis bestätigt werden soll.. Ungefähr 270 erwachsene Teilnehmer mit rezidiviertem/refraktärem MM werden an etwa 45 Standorten weltweit in die Studie aufgenommen. Die Teilnehmer erhalten ABBV-383 intravenös (i.v.) in Kombination mit oral/i.v. verabreichtem Pd, oral/i.v. verabreichtem Rd, oral/i.v./subkutan (s.c.) verabreichtem Dd oder oral/i.v. verabreichtem Niro in 21-tägigen Zyklen.
Für die Teilnehmer an dieser Studie kann die Belastung durch die Behandlung höher sein als bei ihrer Standardbehandlung. Während der Studie werden die Teilnehmer regelmäßig untersucht und die Wirkung und etwaige Nebenwirkungen der Behandlung werden häufig durch medizinische Beurteilungen und Blutuntersuchungen und Fragebögen überprüft.
Hintergrund:
ABBV-383 ist ein Prüfpräparat, das für die Behandlung des rezidivierenden/refraktären Multiplen Myeloms entwickelt wird. Es ist ein Antikörper, der (wie Elranatamab und Teclistamab) gegen zwei Ziele gerichtet (bispezifisch) ist: gegen BCMA und gegen CD3. BCMA ist ein Zelloberflächenprotein, das besonders auf Myelom- und Plasmazellen vorkommt und eine besondere biologische Bedeutung für das Überleben der Plasmazelle hat. Es wird bei Menschen mit Multiplem Myelom in signifikant höherem Maße exprimiert. CD3 ist an der Aktivierung der Immunantwort zur Bekämpfung von Infektionen beteiligt.
.
Ein- und Ausschlusskriterien (Auswahl):
Einschlusskriterien:
- Dokumentierte Diagnose eines Multiplen Myeloms gemäß den IMWG-Diagnosekriterien
- ECOG (Index zur Abstufung der Lebensqualität von Patienten mit Krebserkrankungen) von 0, 1 oder2
- Es muss eine bestätigte Diagnose eines rezidivierten/refraktären Multiplen Myeloms (MM) mit dokumentierten Hinweisen auf ein Fortschreiten der Erkrankung während oder nach der letzten Behandlung des Teilnehmers vorliegen, wie vom Prüfarzt anhand der Kriterien der International Myeloma Working Group (IMWG) ermittelt wurde.
- Es muss eine messbare Erkrankung vorliegen, wie im Prüfplan dargelegt.
- Teilnehmer sind bislang nicht mit ABBV-383 vorbehandelt und haben noch nie eine BCMA-gerichtete Therapie erhalten. Teilnehmer, die eine zielgerichtete Therapie gegen Nicht-BCMA-Targets erhalten haben, werden nicht ausgeschlossen.
Ausschlusskriterien:
- Periphere autologe Stammzelltransplantation (SZT) innerhalb von 12 Wochen oder allogene SZT innerhalb eines Jahres vor der ersten Gabe des Studienmedikaments.
- Fortbestehende unerwünschte Ereignisse ≥ Grad 2 (National Cancer Institute [NCI] Common Terminology Criteria for Adverse Events [CTCAE] Version 5.0) infolge einer früheren Krebstherapie.
- Bekannter Myelombefall des zentralen Nervensystems.
Alle weiteren Kriterien besprechen Sie bitte mit Ihrem behandelnden Arzt
Studie zu Elranatamab als Monotherapie und Elranatamab + Daratumumab im Vergleich zu Daratumumab + Pomalidomid + Dexamethason bei Teilnehmern mit rezidiviertem/refraktärem Multiplem Myelom
Organisatorische Daten:
| Prüfplancode: | C1071005, MagnetisMM-5 |
| ISRCTN: | |
| EudraCT: | 2021-000044-22 |
| Clinicaltrials.gov: | NCT05020236 |
| DRKS: | |
| Sponsor: | Pfizer |
| Studienphase: | Phase 3 |
| Status: | Rekrutierung läuft, geplant bis Okt. 2024 |
Ziel:
Mit dieser Studie soll untersucht werden, ob der bispezifische BCMA/CD3-Antikörper Elranatamab allein und/oder in Kombination mit dem monoklonalen Anti-CD38-Antikörper Daratumumab für Patienten mit Multiplem Myelom einen größeren Nutzen bringt als eine Kombinationstherapie aus Daratumumab, Pomalidomid und Dexamethason.
Hintergrund:
Der bispezifische BCMA/CD3-Antikörper Elranatamab (PF-06863135) zeigte bei Patienten mit rezidiviertem/refraktärem Multiplem Myelom eine vielversprechende vorläufige Wirksamkeit und Verträglichkeit.
Daten aus der Phase-1-Studie MagnetisMM-1 (NCT03269136), die auf der ASCO-Jahrestagung 2021 vorgestellt wurden, zeigten, dass Elranatamab in Dosen von bis zu 1000 µg/kg ein überschaubares Sicherheitsprofil ohne dosislimitierende Toxizitäten aufweist.
Darüber hinaus erzielte der Wirkstoff bei Dosierungen von 215 µg/kg und höher eine Gesamtansprechrate (ORR) von 70 % und eine vollständige Ansprechrate (CR)/stringente CR von 30 %. Bei der empfohlenen Phase-2-Dosis von 1000 µg/kg erzielte der Wirkstoff eine ORR von 83,3 %. Bemerkenswert ist, dass drei von vier in die Studie aufgenommenen Patienten, die zuvor mit einer BCMA-gerichteten Therapie behandelt worden waren, ein Ansprechen erzielten.
Durchführung:
In die Studie werden Patienten mit Multiplem Myelom aufgenommen, die zuvor mit Lenalidomid und einem Proteasom-Inhibitor behandelt wurden.
In Teil 1 der Studie wird die Sicherheit und Wirksamkeit verschiedener Dosen von Elranatamab in Kombination mit Daratumumab untersucht.
Die Teilnehmer an Teil 2 der Studie werden nach dem Zufallsprinzip einer von drei Behandlungsgruppen zugeteilt.
- Teilnehmer in Gruppe 1 erhalten Elranatamab allein als Injektion unter die Haut.
- Teilnehmer der Gruppe 2 erhalten Elranatamab und Daratumumab als Injektion unter die Haut.
- Teilnehmer der Gruppe 3 erhalten die Standardtherapie Daratumumab als Injektion unter die Haut sowie Pomalidomid und Dexamethason zur Einnahme.
In Teil 2 wird die Sicherheit und Aktivität von (1) Elranatamab allein im Vergleich zu Daratumumab, Pomalidomid und Dexamethason und (2) Elranatamab plus Daratumumab im Vergleich zu Daratumumab, Pomalidomid und Dexamethason verglichen. Die Teilnehmer beider Studienteile erhalten die Studienbehandlung so lange, bis ihre Krankheit fortschreitet, unannehmbare Nebenwirkungen auftreten oder sie sich entscheiden, nicht weiter an der Studie teilzunehmen.
Einschlusskriterien:
- Diagnose eines Multiplen Myeloms gemäß den von der International Myeloma Working Group (IMWG) aufgestellten Diagnosekriterien )
- Messbare Erkrankung, definiert durch mindestens 1 der folgenden Punkte:
- M-Protein im Serum > 0,5 g/dl durch SPEP
- M-Protein-Ausscheidung im Urin > 200 mg/24 Stunden mittels UPEP
- Freie Immunglobulin-Leichtketten (FLC) im Serum ≥ 10 mg/dl (≥ 100 mg/l) UND abnormes Verhältnis der Immunglobuline Kappa-zu-Lambda-FLC-im Serum
- Vorherige Therapie gegen multiples Myelom, einschließlich Behandlung mit Lenalidomid und einem Proteasom-Inhibitor.
- ECOG Performance Status (Index zur Abstufung der Lebensqualität von Patienten mit Krebserkrankungen) von 0, 1 oder 2.
Ausschlusskriterien:
- Schwelendes Multiples Myelom
- Aktive Plasmazellleukämie
- Amyloidose
- POEMS-Syndrom
- Stammzelltransplantation innerhalb von 12 Wochen vor der Aufnahme in die Studie
Alle weiteren Kriterien besprechen Sie bitte mit Ihrem behandelnden Arzt
Phase 3- Studie zu Teclistamab
Eine Studie zu Teclistamab in Kombination mit Lenalidomid und Teclistamab allein im Vergleich zu Lenalidomid allein bei Teilnehmern mit neu diagnostiziertem Multiplem Myelom als Erhaltungstherapie nach autologer Stammzelltransplantation (MajesTEC-4)
Organisatorische Daten:
| Prüfplancode: | EMN30/64007957MMY3003 |
| ISRCTN: | |
| EudraCT: | |
| Clinicaltrials.gov: | NCT05243797 |
| DRKS: | |
| Sponsor: | Janssen |
| Studienphase: | Phase 3 |
| Status: | Rekrutierung läuft, geplant bis Oktober 2028 |
Ziele:
Ziel dieser Studie ist es, den Nutzen von Teclistamab in Kombination mit Lenalidomid und von Teclistamab als Monotherapie im Vergleich zu einer Monotherapie mit Lenalidomid bei Patienten mit Multiplem Myelom nach einer autologen Stammzelltherapie zu überprüfen.
Hintergrund:
Teclistamab ist ein bispezifischer Antikörper, der sowohl gegen das B-Zell-Reifungsantigen (BCMA), ein Protein auf Myelomzellen, als auch gegen CD3-Rezeptoren auf der T-Zell-Oberfläche gerichtet ist. Teclistamab wurde im August 2022 in der EU als Monotherapie zur Behandlung des fortgeschrittenen Multiplen Myeloms zugelassen und wird jetzt bei weiteren Indikationen geprüft.
In der MajesTEC-1-Studie bei stark vorbehandelten Patienten mit Multiplem Myelom (n=165) bewirkte Teclistamab ein hohes und dauerhaftes Ansprechen. Bei einer medianen Nachbeobachtungszeit von etwa 14 Monaten betrug die Gesamtansprechrate 63 Prozent, wobei 39,4 Prozent ein komplettes Ansprechen oder besser erreichten. Diese Daten wurden auf der Jahrestagung 2022 der American Society of Clinical Oncology (ASCO) veröffentlicht.
Ein- und Ausschlusskriterien (Auswahl):
Einschlusskriterien:
- Neu diagnostiziertes Multiples Myelom gemäß den Diagnosekriterien der International Myeloma Working Group (IMWG) und Erhalt einer Induktionstherapie mit oder ohne Konsolidierung
- Erhalt nur einer Therapielinie und Erreichen eines mindestens partiellen Ansprechens gemäß den IMWG-Ansprechkriterien ohne Anzeichen einer Progression zum Zeitpunkt der ersten Gabe der Studienmedikation
- ECOG-Performance-Status-Score (Index zur Abstufung der Lebensqualität von Patienten mit Krebserkrankungen) von 0, 1 oder 2 beim Screening und unmittelbar vor Beginn der Verabreichung der Studienmedikation
Ausschlusskriterien:
- Unverträglichkeit gegenüber der Anfangsdosis von Lenalidomid
- Erhaltungstherapie
- Vorherige gegen das B-Zell-Reifungsantigen (BCMA) gerichtete Therapie
- Vorherige Therapie mit einem Mittel, das Immunzellen neu ausrichtet, oder einer gentechnisch veränderten adoptiven Zelltherapie (z. B. mit chimärem Antigenrezeptor-modifizierte T-Zellen, NK-Zellen)
- Abbruch der Behandlung aufgrund einer Nebenwirkung von Lenalidomid, bei der der Prüfarzt einen Zusammenhang mit Lenalidomid sieht
- Fortschreiten des Multiplen Myeloms zu irgendeinem Zeitpunkt vor dem Screening
- Erhalt einer kumulativen Kortikosteroid-Dosis, die ≥ 140 mg Prednison entspricht, in den 14 Tagen vor der ersten Behandlungsdosis
- Impfung mit einem abgeschwächten Lebendimpfstoff innerhalb von 4 Wochen vor der ersten Behandlungsdosis. Totimpfstoffe und nicht replizierende, für den Notfall zugelassene Impfstoffe sind erlaubt.
Alle weiteren Kriterien besprechen Sie bitte mit Ihrem behandelnden Arzt
Talquetamab
Talquetamab in Kombination mit Daratumumab oder in Kombination mit Daratumumab und Pomalidomid im Vergleich zu Daratumumab in Kombination mit Pomalidomid und Dexamethason bei Teilnehmern mit rezidiviertem oder refraktärem Multiplem Myelom (MonumenTAL-3)
Organisatorische Daten:
| Prüfplancode: | CR109082, 64407564MMY3002 |
| ISRCTN: | |
| EudraCT: | 2021-000202-22 |
| Clinicaltrials.gov: | NCT05455320 |
| DRKS: | |
| Sponsor: | Janssen |
| Studienphase: | 3 |
| Status: | Rekrutierung geplant bis Febr 2029 |
Ziel:
Ziel der Studie ist der Vergleich der Wirksamkeit von unter die Haut (subkutan, s.c.) verabreichtem Talquetamab in Kombination mit Daratumumab s.c. und Pomalidomid (Tal-DP) bzw. Talquetamab s.c. in Kombination mit Daratumumab s.c. (Tal-D) gegenüber Daratumumab s.c. in Kombination mit Pomalidomid und Dexamethason (DPd) bei Teilnehmern mit rezidiviertem oder refraktärem Multiplem Myelom, die mindestens eine vorherige Therapielinie erhalten haben.
Hintergrund:
Talquetamab ist ein humanisierter monoklonaler Antikörper, der gegen zwei Ziele gerichtet (bispezifisch) ist: gegen humanes CD3, ein Oberflächenantigen auf T-Zellen, und gegen GPRC5D (G protein-coupled receptor family C group 5 member D), ein Antigen in Tumorzellen oder auf deren Oberfläche (tumor-assoziiertes Antigen). Bei Verabreichung bindet Talquetamab sowohl an CD3 auf T-Zellen als auch an GPRC5D, das auf bestimmten Tumorzellen wie z.B. dem Multiplen Myelom vermehrt vorkommt und eine Schlüsselrolle bei der Vermehrung von Tumorzellen spielt.
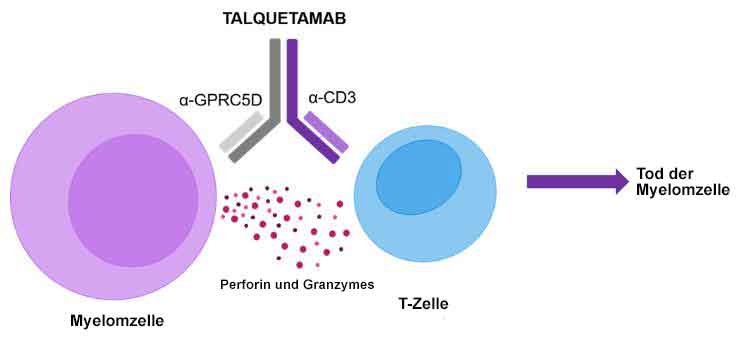
Abb. aus https://multiplemyelomahub.com/,
Durchführung:
Die Studie ist in drei Phasen unterteilt: Voruntersuchung (Screening), Behandlung (bis eines der folgenden Ereignisse eintritt: bestätigtes Fortschreiten der Krankheit, Tod, unverträgliche Toxizität, Widerruf der Einwilligung oder Ende der Studie) und Nachbeobachtung (bis eines der folgenden Ereignisse eintritt: Tod, Widerruf der Einwilligung, Verlust der Nachbeobachtung oder Ende der Studie). Wirksamkeit, Sicherheit, Pharmakokinetik, Immunogenität und Biomarker werden zu bestimmten Zeitpunkten untersucht. Die Gesamtdauer der Studie beträgt bis zu 6 Jahren und 6 Monaten.
Ein- und Ausschlusskriterien (Auswahl):
Einschlusskriterien:
- Dokumentiertes Multiples Myelom, definiert als
- a) Diagnose des Multiplen Myeloms gemäß den diagnostischen Kriterien der International Myeloma Working Group (IMWG) und
- b) messbare Erkrankung zum Zeitpunkt des Screenings gemäß der Definition im Protokoll
- Rezidivierte oder refraktäre Erkrankung gemäß folgender Definition:
- eine rezidivierte Erkrankung ist definiert als anfängliches Ansprechen auf die vorherige Behandlung, gefolgt von einer nach IMWG-Kriterien bestätigten fortschreitenden (progredienten) Erkrankung mehr als 60 Tage nach Beendigung der Behandlung;
- eine refraktäre Erkrankung ist definiert als eine Verringerung des monoklonalen Paraproteins (M-Protein) um weniger als 25 % oder eine nach IMWG-Kriterien bestätigte fortschreitende Erkrankung während der vorherigen Behandlung oder ≤ 60 Tage nach Beendigung der Behandlung
- Teilnehmer müssen mindestens eine vorherige Linie einer Myelom-Therapie, einschließlich eines Proteasom-Inhibitors (PI) und Lenalidomid, erhalten haben. Patienten, die nur eine vorherige Linie einer Myelom-Therapie erhalten haben, müssen als Lenalidomid-refraktär gelten (d. h. bei ihnen ist bei Beendigung einer Lenalidomid-haltigen Therapie oder innerhalb von 60 Tagen danach eine fortschreitende (progrediente) Erkrankung nach IMWG-Kriterien nachweisbar). Teilnehmer, die 2 oder mehr vorherige Therapielinien zur Behandlung des Myeloms erhalten haben, müssen als Lenalidomid-behandelt gelten
- Dokumentierte Anzeichen einer fortschreitenden Erkrankung, basierend auf der Feststellung des Ansprechens durch den Prüfarzt gemäß den IMWG-Kriterien während oder nach der letzten Behandlung
- ECOG (Index zur Abstufung der Lebensqualität von Patienten mit Krebserkrankungen) von 0, 1 oder 2
Ausschlußkriterien
- Gegenanzeigen oder lebensbedrohliche Allergien, Überempfindlichkeiten oder Unverträglichkeiten gegenüber Hilfsstoffen des Studienmedikaments
- Refraktär gegenüber einem monoklonalen Antikörper gegen Cluster of Differentiation 38 (CD38), wie in den IMWG-Konsensrichtlinien definiert (Fortschreiten der Erkrankung während der Behandlung oder innerhalb von 60 Tagen nach Beendigung der Therapie mit einem monoklonalen Antikörper gegen CD38)
- Erhalt von Kortikosteroiden in einer maximalen Gesamtdosis von oder entsprechend ≥ 140 mg Prednison innerhalb von 14 Tagen vor Gabe der ersten Dosis des Studienmedikaments
- Bekannte aktive Beteiligung des zentralen Nervensystems (ZNS) oder klinische Anzeichen einer meningealen Beteiligung des Multiplen Myeloms. Bei Verdacht auf eine der beiden Erkrankungen sind eine negative Magnetresonanztomographie (MRT) des gesamten Gehirns und eine lumbale Zytologie erforderlich.
- Plasmazellleukämie zum Zeitpunkt der Voruntersuchung, Waldenström-Makroglobulinämie, Polyneuropathie, Organomegalie, Endokrinopathie, M-Protein und Hautveränderungen (POEMS-Syndrom) oder primäre Amyloid-Leichtketten-Amyloidose
Alle weiteren Kriterien besprechen Sie bitte mit Ihrem behandelnden Arzt.
Erstanwendung von REGN5458 am Menschen bei Patienten mit rezidiviertem oder refraktärem Multiplem Myelom (MM)
Organisatorische Daten:
| Prüfplancode: | R5458-ONC-1826 |
| ISRCTN: | |
| EudraCT: | 2018-003188-78 |
| Clinicaltrials.gov: | NCT03761108 |
| DRKS: | |
| Sponsor: | Regeneron Pharmaceuticals |
| Studienphase: | Phase 1/2 Erstanwendung am Menschen |
| Status: | Rekrutierung läuft, geplant bis Mai 2025 |
Ziele:
Im Phase-1-Teil der Studie: Bewertung der Sicherheit, Verträglichkeit und dosisbegrenzender Nebenwirkungen (dosislimitierender Toxizitäten) und Ermittlung eines für die Phase 2 empfohlenen Dosierungsschemas von REGN5458 als Monotherapie bei Patienten mit rezidiviertem oder refraktärem multiplem Myelom.
Im Phase-2-Teil der Studie: Bewertung der Anti-Tumor-Aktivität von REGN5458, gemessen an der objektiven Ansprechrate und bestimmt durch ein unabhängiges Prüfungskomitee.
Hintergrund:
REGN5458 ist ein Antikörper, der gegen zwei Ziele gerichtet (bispezifisch) ist. Er soll an das Oberflächenprotein BCMA (B-cell maturation antigen) auf multiplen Myelomzellen und an den CD3-Rezeptor auf T-Zellen binden, um sie miteinander zu verbinden und die T-Zellen zur Abtötung der Krebszellen zu aktivieren.
Ein- und Ausschlusskriterien (Auswahl):
Einschlusskriterien:
- ECOG Performance Status (Index zur Abstufung der Lebensqualität von Patienten mit Krebserkrankungen) von 0 oder 1.
- Bestätigte Diagnose eines aktiven Multiplen Myeloms gemäß den von der International Myeloma Working Group (IMWG) aufgestellten Diagnosekriterien
- Das Ansprechen muss anhand der Ansprechkriterien der IMWG auswertbar sein.
-
Phase 1 Dosissteigerung:
- Patienten mit MM, die alle Behandlungsmöglichkeiten ausgeschöpft haben, von denen ein bedeutsamer klinischer Nutzen zu erwarten ist, was sich entweder durch einen Krankheitsrückfall, eine behandlungsrefraktäre Erkrankung oder eine Unverträglichkeit der Therapie zeigt und einen der folgenden Punkte umfasst:
- Fortschreiten der Erkrankung während oder nach mindestens drei Therapielinien oder Unverträglichkeit der Therapie, einschließlich eines Proteasom-Inhibitors, eines immunmodulatorischen Wirkstoffs (IMiD) und eines Anti-CD38-Antikörpers ODER
- Fortschreiten der Krankheit während oder nach einem Anti-CD38-Antikörper und „doppelte Refraktärität“ gegenüber einem Proteasom-Inhibitor und einem IMiD oder Unverträglichkeit der Therapie. Der Anti-CD38-Antikörper kann allein oder in Kombination mit einem anderen Wirkstoff, z. B. einem Proteasom-Inhibitor, verabreicht worden sein. Eine refraktäre Erkrankung ist definiert als Ausbleiben des Ansprechens oder Rückfall innerhalb von 60 Tagen nach der letzten Behandlung.
Phase 2:
- Die Patienten müssen dreifach refraktär sein, d. h. sie müssen auf eine vorherige Behandlung mit mindestens einem Anti-CD38-Antikörper, einem Proteasom-Inhibitor und einem IMiD refraktär sein. Darüber hinaus müssen die Patienten fünf Wirkstoffe erhalten haben (d. h. sie müssen zuvor mit zwei Proteasom-Inhibitoren, zwei IMiDs [Lenalidomid und Pomalidomid] und einem monoklonalen Anti-CD38-Antikörper behandelt worden sein).
Ausschlusskriterien:
- Diagnose einer Plasmazellleukämie, einer primären systemischen Leichtketten-Amyloidose (ausgenommen Myelom-assoziierte Amyloidose), einer Waldenström-Makroglobulinämie (lymphoplasmatisches Lymphom) oder eines POEMS-Syndroms (Polyneuropathie, Organomegalie, Endokrinopathie, monoklonale Proteine und Hautveränderungen)
- Patienten mit bekannten MM-Hirnläsionen oder meningealer Beteiligung
- Vorherige Behandlung mit BCMA-gerichteten Immuntherapien, einschließlich BCMA-bispezifischer Antikörper und BiTEs sowie BCMA-CAR-T-Zellen.
- Hinweis: BCMA-Antikörper-Wirkstoff-Konjugate sind nicht ausgeschlossen
- Vorgeschichte einer allogenen Stammzelltransplantation zu irgendeinem Zeitpunkt oder einer autologen Stammzelltransplantation innerhalb von 12 Wochen vor Beginn der Studienbehandlung
Alle weiteren Kriterien besprechen Sie bitte mit Ihrem behandelnden Arzt
Subkutanes Daratumumab-Regime in Kombination mit Talquetamab oder Teclistamab zur Behandlung von Patienten mit rezidiviertem oder refraktärem Multiplem Myelom (TRIMM-2)
Organisatorische Daten:
| Prüfplancode: | |
| ISRCTN: | |
| EudraCT: | 2019-000330-19 |
| Clinicaltrials.gov: | NCT04108195 |
| DRKS: | |
| Sponsor: | Janssen |
| Studienphase: | I |
| Status: | Rekrutierung läuft, |
Ziel:
Mit dieser Studie sollen die Sicherheit von Daratumumab in Kombination mit Talquetamab oder Teclistamab sowie die vorläufige Antitumoraktivität jeder Kombination bewertet werden.
Durchführung:
Die Studie besteht aus mehreren Zeiträumen: Voruntersuchung (Screening), Behandlung (Teil 1 und 2) und Nachbeobachtung(nach Behandlungsende und bis zu 16 Wochen nach der letzten Dosis). In Teil 1 der Behandlung erhalten Patienten eine der folgenden Kombinationen in steigender Dosierung (Dosiseskalation):
- Daratumumab plus Teclistamab oder
- Daratumumab plus Talquetamab oder
- Daratumumab plus Talquetamab plus Pomalidomid oder
- Daratumumab plus Teclistamab plus Pomalidomid.
In Teil 2 der Behandlung erhalten Patienten die für die Phase 2 empfohlene Dosis, die in Teil 1 für ausgewählte Kombinationen ermittelt wurde (Dosisexpansion).
Das Studienende ist definiert als letzte Studienbeurteilung des letzten Studienteilnehmers. Die Gesamtdauer der Studie beträgt etwa 2,4 Jahre. Wirksamkeit, Sicherheit, Pharmakokinetik (PK), Immunogenität und Biomarker werden zu festgelegten Zeitpunkten bewertet. Die Sicherheit der Teilnehmer wird während der gesamten Studie überwacht.
Hintergrund:
Diese Studie beruht auf der Annahme, dass Daratumumab in Kombination mit Talquetamab oder Teclistamab aufgrund verschiedener Wirkungsmechanismen zu verbesserten klinischen Reaktionen bei der Behandlung des rezidivierten oder refraktären Multiplen Myeloms führen kann.
Daratumumab ist ein humaner monoklonaler Immunglobulin-G1-kappa-Antikörper (IgG1k), der mit hoher Affinität an CD38 (ein Oberflächenmolekül) bei einer Vielzahl von hämatologischen Malignomen einschließlich des Multiplen Myeloms bindet. Talquetamab und Teclistamab sind gegen zwei Ziele gerichtete (bispezifische) T-Zell-Redirektions-Antikörper. Talquetamab bindet an den CD3-Rezeptorkomplex auf T-Zellen und an die G-Protein-gekoppelte Rezeptorfamilie CGPRC5D, ein 7-Transmembran-Rezeptorprotein auf Plasmazellen. Teclistamab bindet an humanes und Cynomolgus-CD3- und B-Zell-Reifungsantigen (BCMA).
Einschlusskriterien:
- Dokumentierte Erstdiagnose eines Multiplen Myeloms nach den Diagnosekriterien der Internationalen Myelom-Arbeitsgruppe (IMWG)
- Einer der folgenden Punkte muss vorliegen
-
- a) mindestens 3 vorherige Therapielinien einschließlich eines Proteasom-Inhibitors (PI) (mindestens 2 Zyklen oder 2 Monate Behandlung) und eines immunmodulatorischen Medikaments (IMiD) (mindestens 2 Zyklen oder 2 Monate Behandlung) in beliebiger Reihenfolge während der Behandlung oder
- b) Krankheit, die weder auf einen PI noch ein IMiD anspricht (doppelt refraktär)
- Messbare Erkrankung beim Screening gemäß der Definition im Protokol
- ECOG (Index zur Abstufung der Lebensqualität von Patienten mit Krebserkrankungen) von 0 oder 1
Ausschlusskriterien:
- Behandlung in den vorangegangenen 3 Monaten mit einer Anti-CD38-Therapie (z.B. Daratumumab) oder Abbruch einer vorherigen Anti-CD38-Therapie zu einem beliebigen Zeitpunkt aufgrund eines unerwünschten Ereignisses im Zusammenhang mit der Anti-CD38-Therapie
- Attenuierter Lebendimpfstoff innerhalb von 4 Wochen vor der ersten Dosis des Studienmedikaments, sofern nicht vom Sponsor genehmigt
- Aktive Beteiligung des Zentralnervensystems oder klinische Anzeichen einer Hirnhautbeteiligung des Multiplen Myeloms. Bei Verdacht auf eines von beiden sind eine Magnetresonanztomographie (MRT) des Gehirns und eine Lumbal-Zytologie erforderlich.
Alle weiteren Kriterien besprechen Sie bitte mit Ihrem behandelnden Arzt.
Eine Studie mit Talquetamab und Teclistamab jeweils in Kombination mit einem PD-1-Inhibitor (Programmed Cell Death Receptor-1) zur Behandlung von Teilnehmern mit rezidiviertem oder refraktärem Multiplem Myelom (TRIMM-3)
Organisatorische Daten:
| Prüfplancode: | CR109168, 64407564MMY1005 |
| ISRCTN: | |
| EudraCT: | 2021-005073-22 |
| Clinicaltrials.gov: | NCT05338775 |
| DRKS: | |
| Sponsor: | Janssen |
| Studienphase: | 1 |
| Status: | Rekrutierung läuft, geplant bis Sept. 2024 |
Ziel:
Ziel der Studie ist es, die sichere Dosis bzw. sicheren Dosen eines PD-1-Inhibitors in Kombination mit Talquetamab oder Teclistamab zu ermitteln und die Sicherheit und Verträglichkeit von Talquetamab oder Teclistamab bei Verabreichung in Kombination mit einem PD-1-Inhibitor zu charakterisieren.
Hintergrund:
Talquetamab ist ein humanisierter monoklonaler Antikörper, der gegen zwei Ziele gerichtet (bispezifisch) ist: gegen humanes CD3, ein Oberflächenantigen auf T-Zellen, und gegen GPRC5D, ein Antigen in Tumorzellen oder auf deren Oberfläche (tumor-assoziiertes Antigen). Bei Verabreichung bindet Talquetamab sowohl an CD3 auf T-Zellen als auch an GPRC5D, das auf bestimmten Tumorzellen wie z.B. dem Multiplen Myelom vermehrt vorkommt und eine Schlüsselrolle bei der Vermehrung von Tumorzellen spielt.
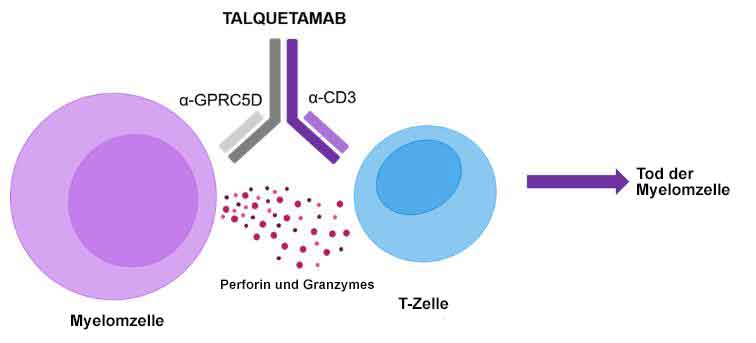
Abb. aus https://multiplemyelomahub.com/,
Teclistamab (JNJ-7957) ist ein bispezifischer Antikörper, der sowohl gegen BCMA als auch gegen CD3 gerichtet ist. BCMA ist ein Zelloberflächenprotein, das besonders auf Myelom- und Plasmazellen vorkommt und eine besondere biologische Bedeutung für das Überleben der Plasmazelle hat. Es wird bei Menschen mit Multiplem Myelom in signifikant höherem Maße exprimiert. CD3 ist an der Aktivierung der Immunantwort zur Bekämpfung von Infektionen beteiligt, Teclistamab lenkt CD3-T-Zellen auf BCMA-exprimierende Myelomzellen um, um die Zytotoxizität der Zielzellen zu induzieren. Ergebnisse aus präklinischen Studien zeigen, dass Teclistamab Myelom-Zelllinien und Myelom-Knochenmarkzellen von stark vorbehandelten Patienten abtötet.
Diese Studie geht davon aus, dass Talquetamab oder Teclistamab in Kombination mit einem PD-1-Inhibitor bei der Behandlung von rezidiviertem oder refraktärem Multiplem Myelom zu einem verbesserten klinischen Ansprechen führen, was auf verschiedene Wirkmechanismen zurückzuführen ist.
Einschlusskriterien:
- Dokumentierte Erstdiagnose eines Multiplen Myeloms nach den Diagnosekriterien der Internationalen Myelom-Arbeitsgruppe (IMWG)
- Teilnehmer mit rezidivierender oder refraktärer Erkrankung, die nicht für eine verfügbare Therapie mit nachgewiesenem klinischen Nutzen infrage kommen.
- Messbare Erkrankung zum Zeitpunkt des Screenings
- ECOG (Index zur Abstufung der Lebensqualität von Patienten mit Krebserkrankungen) von 0 oder 1
Ausschlusskriterien:
-
Vorangegangene Antitumortherapie innerhalb von 21 Tagen vor der ersten Dosis der Studienbehandlung (Therapie mit Proteasom-Inhibitoren [PI] oder Strahlentherapie innerhalb von 14 Tagen, Therapie mit immunmodulatorischen Wirkstoffen (IMiD) innerhalb von 7 Tagen, genmodifizierte adoptive Zelltherapie oder autologe Stammzelltransplantation innerhalb von 3 Monaten)
-
Vorherige Therapie mit PD-1-Inhibitoren, allogene Stammzelltransplantation oder Organtransplantation
-
Aktive Plasmazellleukämie, Waldenstrom-Makroglobulinämie, POEMS-Syndrom (Polyneuropathie, Organomegalie, Endokrinopathie, M-Protein und Hautveränderungen) oder primäre Leichtkettenamyloidose
-
Aktive Beteiligung des zentralen Nervensystems (ZNS) oder klinische Anzeichen einer meningealen Beteiligung des Multiplen Myeloms. Bei Verdacht auf eine der beiden Erkrankungen sind eine Magnetresonanztomographie des Gehirns (MRT) und eine Lumbalzytologie erforderlich.
-
Impfung mit einem abgeschwächten Lebendimpfstoff innerhalb von 4 Wochen vor der ersten Dosis der Studienbehandlung
Alle weiteren Kritereien besprechen Sie mit Ihrem Arzt
Zusätzliche Information
Sitz der Deutschen Studiengruppe Multiples Myelom (DSMM)
Onkologische Gemeinschaftspraxis Dr. Schlag / Dr. Schöttker, Stiftung Juliushospital Würzburg
0931-393-0
Unterkategorien
-
Aschaffenburg
- COM_STUDIES_NUM
- 3
-
Augsburg
- COM_STUDIES_NUM
- 3
-
Bamberg
- COM_STUDIES_NUM
- 1
-
Coburg
- COM_STUDIES_NUM
- 1
-
Erlangen
- COM_STUDIES_NUM
- 1
-
Landshut
- COM_STUDIES_NUM
- 1
-
München
- COM_STUDIES_NUM
- 8
-
Freising
- COM_STUDIES_NUM
- 1
-
Fürth
- COM_STUDIES_NUM
- 1
-
Neumarkt i.d.O.
- COM_STUDIES_NUM
- 1
-
Germering
- COM_STUDIES_NUM
- 1
-
Nürnberg
- COM_STUDIES_NUM
- 1
-
Regensburg
- COM_STUDIES_NUM
- 2
-
Hof
- COM_STUDIES_NUM
- 1
-
Kempten
- COM_STUDIES_NUM
- 1
-
Traunstein
- COM_STUDIES_NUM
- 1
-
Weiden
- COM_STUDIES_NUM
- 1
-
Würzburg
- COM_STUDIES_NUM
- 2
-
Bayreuth
- COM_STUDIES_NUM
- 1
-
Rosenheim
- COM_STUDIES_NUM
- 1
-
Amberg
- COM_STUDIES_NUM
- 1

